文献分享:多重免疫组化与免疫荧光技术实践进展
发表时间:2026-01-21一、研究背景
近年来,肿瘤微环境(TME)的复杂免疫景观解析成为精准肿瘤学的研究核心,而常规临床仍依赖 H&E 染色和单一标志物显色 IHC 检测,该方法存在组织浪费、无法同步评估多标志物、不适用于定量和空间分析等局限,难以满足肿瘤微环境研究及免疫治疗响应预测需求。肿瘤微环境的细胞丰度与空间排列影响肿瘤进展及治疗响应,单一 IHC 评估 PD-L1 表达预测免疫治疗响应时,存在可重复性差、无法明确表达细胞类型及定量空间排列等问题,而多重染色能同步靶向多种蛋白质,通过荧光或显色染色实现,可表征标志物共表达谱和空间排列,在预测免疫治疗响应上优于多种检测方法,且在肿瘤微环境研究、生物标志物空间异质性分析、解决小样本多标志物检测难题及临床试验患者分层等方面具有广泛应用价值,其优化和实施难度不断降低,更适合常规临床使用。《Multiplex Immunohistochemistry and Immunofluorescence: A Practical Update for Pathologists》是一篇面向病理医师的综述类文献,聚焦多重免疫组织化学(mIHC)与多重免疫荧光(mIF)技术,聚焦多重免疫组织化学(mIHC)与多重免疫荧光(mIF)技术,通过在同一切片上同时检测多个生物标志物,极大地提升了病理诊断的信息量与精准度。目前,实现多重检测的技术路径主要包括基于 TSA 等方法的多重 IHC / 免疫荧光、质谱成像及数字空间分析(DSP),以及通过连续切片配准实现的虚拟多重染色。尽管这些技术在标准化流程与数据分析方面仍面临挑战,但随着数字病理技术的成熟,多重染色已逐渐具备临床转化的可行性,有望在不久的将来成为指导肿瘤免疫治疗决策的常规手段。
二、常规单重和双重组织染色
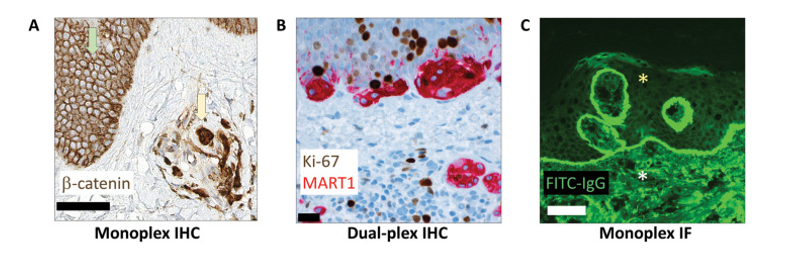
单一显色免疫组织化学
单重显色 IHC 用于在明场显微镜下以单一颜色检测组织中某一种抗原。其原理是通过直接或间接酶联抗体策略,使底物在抗原位置显色,并借助复染显示组织背景,从而判断目标抗原的定位与表达情况。
传统上,单重IHC一直是诊断病理学的首选方法,因技术成熟、成本较低、操作简便、周转时间短、染色玻片可永久存档并可在光学显微镜下结合形态学进行判读而被广泛应用,同时也已有完善的临床验证指南,部分标志物还可借助图像算法进行定量分析;然而,单重 IHC 仍存在明显局限性,包括主要依赖病理学家的半定量人工判读,易产生观察者间差异,不同实验室的实验流程差异也会影响结果的重现性,且显色染色的线性动态范围较窄,易出现信号饱和,难以覆盖生物样本中蛋白表达的宽动态范围,因此在需要精确区分低表达水平或进行严格定量的临床场景中存在不足,此外,由于一次只能检测一种标志物,在需要多种标志物联合表型分析时往往依赖连续切片的对比,容易因细胞分布不一致或组织损耗导致难以进行准确的空间定位和共表达分析。为应对这些挑战,许多临床实验室已逐步开展双重标志物检测,部分中心也开始采用商业化平台进行多重明场免疫染色,以在保留形态学背景的同时实现更多靶点的同步分析。
双重显色免疫组织化学
双重显色免疫组织化学通过在同一组织切片染色2种不同标志物实现可视化共同评估,通常以DAB标记一种靶标,萘酚/固红等标记另一种,常规应用包括Ki-67/MART1双重染色评估黑色素细胞病变增殖指数、CD3/CD20双重染色对比免疫浸润中T/B细胞群体、前列腺活检AMACR/p63/高分子量角蛋白区分癌与良性前列腺腺体、p40/napsin A或TTF1/CK5/6区分肺鳞癌与腺癌等临床场景。然而,该技术仍存在明显局限,主要包括显色剂在共定位时易发生颜色叠加形成难以判读的深色信号、抗体物种来源受限,需不同物种一抗以避免交叉反应,以及检测成本相对较高等问题,这些因素在一定程度上限制了其在复杂病理评估中的应用。
免疫荧光
免疫荧光(IF)技术凭借其 5 至 6 个数量级的宽动态范围,能够更真实地反映蛋白表达水平,在理论上比显色 IHC 更适合精准定量(如 HER2 低表达检测)及患者靶向治疗分层,目前临床上主要用于自身免疫性疾病的免疫反应物检测。然而,该技术在常规病理实验室的普及仍受限于诸多因素,包括传统上需在暗室环境下操作、仪器标准化程度低、缺乏形态学复染背景、FFPE 组织的自发荧光干扰以及荧光信号易淬灭难以长期保存等,尽管玻片数字化技术在一定程度上缓解了操作与存档的难题,但抗体物种限制及对 FFPE 样本的适应性仍有待进一步优化。
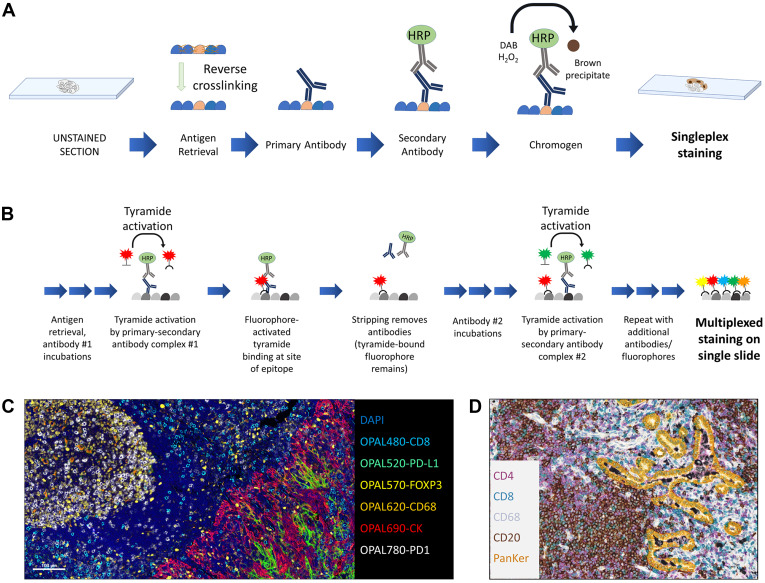
三、多重免疫组织化学染色
多重检测作为能够在同一张组织切片上同时评估两种及以上标志物的技术,尤其是多重免疫荧光,已在肿瘤微环境研究及免疫治疗反应预测中展现出优于传统检测手段的潜力。然而,其向临床转化仍面临诸多技术瓶颈,包括实验方案优化与验证耗时耗力、相同物种抗体来源受限、抗体竞争导致的空间位阻效应、光谱重叠限制可检测靶点数量以及染色顺序与抗原修复对结果的影响,此外,复杂的多重数据往往依赖专业的数字化图像分析才能实现有效解读,这些因素共同制约了其在常规病理诊断中的广泛应用。
使用酪酰胺信号放大的多重免疫荧光
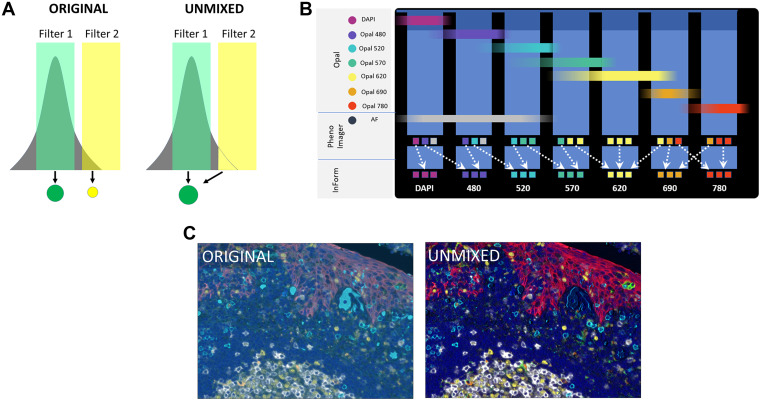
酪酰胺信号放大技术(TSA)的核心原理与传统IHC存在共通性,均依赖酶偶联二抗介导信号传导,但创新性引入了酪酰胺偶联的显色剂或荧光团,其核心优势源于酶促反应的信号放大效应:当偶联酶HRP与酪酰胺发生反应时,会产生活性自由基,驱动显色剂或荧光团以共价键形式稳定结合于抗体结合位点附近的蛋白质上,这种共价结合特性使得后续可通过洗脱步骤去除未结合的抗体,为同一张组织切片上进行多轮抗体孵育与TSA信号标记创造了条件。基于这一特性,TSA技术不仅显著提升了检测灵敏度,尤其适用于低丰度标志物的检出,还可通过搭配不同光谱的荧光团或显色剂实现多靶点同步检测。该技术与常规IHC方案相似,可手动或自动染色,多数临床实验室具备基础技术设施,适配新鲜/冷冻和FFPE组织,可分析大组织切片,玻璃切片上的荧光信号可直接观察用于质量控制或解读,且多种图像分析设备支持定量。但试验区需注意方案优化,如染色顺序、TSA试剂用量影响抗原性和空间位阻、剥离方案。
免疫组织化学循环染色
另一类重要的多重染色策略是显色IHC循环染色技术,其中应用较广泛的是单张玻片多重IHC连续染色法(MICSSS),其技术核心是通过“染色-扫描-化学脱色”的重复循环流程突破单轮染色的靶点限制,在每一轮循环中,先对组织切片进行特定标志物的显色IHC染色,完成后对切片进行数字化扫描存档,再通过化学方法剥离切片上的显色底物与结合抗体,随后进入下一轮针对新标志物的染色-扫描-脱色流程,最终通过数字化图像配准与融合技术,将多轮循环的扫描结果整合为一张多色数字化图像,理论上可实现单次实验检测10种及以上标志物,大幅提升了单张组织切片的信息挖掘效率,尤其适用于需要系统分析多种免疫细胞亚群或信号通路分子共表达模式的研究场景。但该技术的临床应用挑战显著,一方面,循环流程耗时冗长,显著限制了检测通量,难以满足临床常规诊断的高效性需求。另一方面,多次循环中的盖玻片移除、化学脱色及重复抗原修复步骤,极易导致组织样本的抗原性降解、形态结构破坏甚至组织移位,不仅会降低单轮染色的图像质量,还会影响多轮图像配准的精度。同时,该技术对显色剂的可溶性要求极高,仅能选用特定可溶性显色剂,限制了标志物检测的选择范围,且最终获得的仅为数字化多色扫描图,而非可长期存档、反复复核的实体玻片。此外,标志物的表达强度仅能进行半定量评估,难以满足精准医疗对定量数据的需求,这些因素共同制约了其在临床常规诊断中的广泛应用。
虚拟多重技术
作为一种无需复杂实验操作的替代方案,虚拟多重染色(Virtual multiplexing)将样本连续切片的单重显色IHC染色全切片图像数字化,通过软件配准和融合生成多色数字切片,用于视觉评估或数字分析,该技术基于实验室现有染色方案,可规避真实多重染色的技术挑战,病理医师能在H&E扫描切片定位感兴趣区域,快速切换查看同一区域的多重IHC染色结果。然而,该技术本质上仍受限于连续切片的物理特性,由于切片间存在不可避免的细胞丢失与位移,导致不同靶点的空间对应关系难以精确匹配,无法实现真正意义上的共定位分析,且在需要大量切片时面临组织耗竭的风险,使其在依赖精准空间信息的复杂病理评估中仍存在明显局限。
多重图像的分析与解读
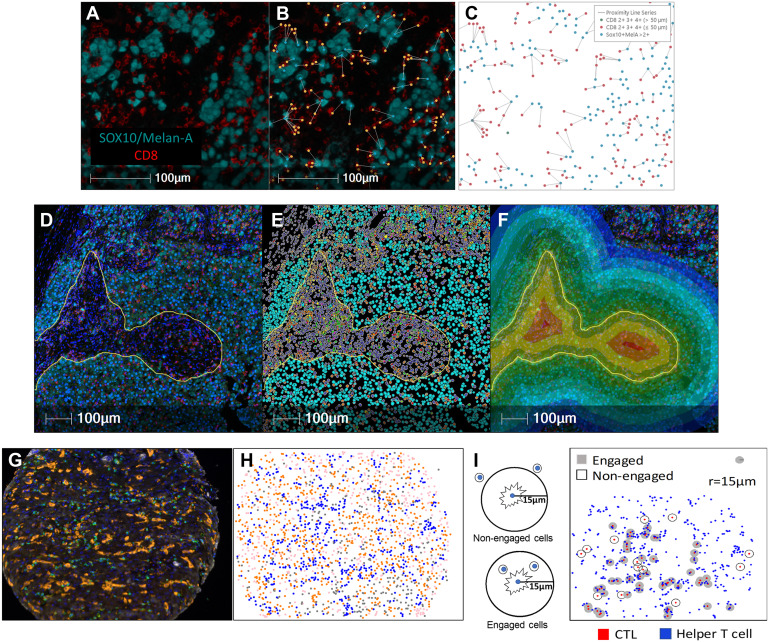
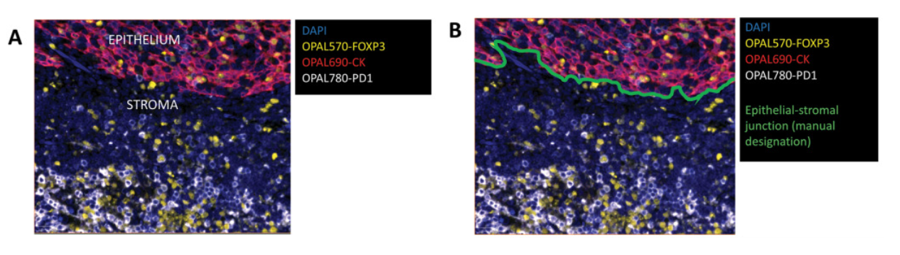
多重图像的解读方式分为直接视觉解读和数字分析两类,其中直接视觉解读适用于肿瘤免疫表型分析等简单任务,低重显色IHC可通过玻璃切片解读,多重IF需数字切片解读则必须依赖数字化图像分析技术。该流程通常始于光谱拆分以消除荧光串扰,并通过定义感兴趣区域聚焦分析范围。随后,主要通过两种核心算法进行数据提取:一种是基于形态学的 细胞分割法,利用核染料识别单个细胞,并结合膜或细胞质信号进行表型分类,适用于细胞计数和邻域分析。另一种是基于分子特征的区室化分析法。,通过像素强度评估特定亚细胞结构或细胞外基质中的蛋白表达,不依赖完整的细胞形态。然而,数字分析仍面临诸多挑战,包括非特异性背景信号干扰、细胞分割算法在处理不规则细胞或细胞核不在切面时的误差,以及基于像素分析难以区分单个细胞的局限性,这些因素均可能影响最终定量结果的准确性。
四、总结
尽管多重检测技术在临床应用中仍处于起步阶段,但其在肿瘤诊断分类及免疫治疗预后评估方面的巨大潜力正推动着该领域的发展。特别是在预后分析中,以 PD-1/PD-L1 及免疫细胞标志物为核心的多重组合已通过临床验证,有望成为指导免疫治疗的伴随诊断工具。在技术路径上,基于 TSA 的明场多重 IHC 因能兼容现有病理工作流,预计将率先在临床实验室得到普及。然而,鉴于单重和双重检测技术的成熟度与成本优势,多重检测在短期内将作为重要补充,而非完全替代传统手段。
参考文献
Harms PW, Frankel TL, Moutafi M, Rao A, Rimm DL, Taube JM, Thomas D, Chan MP, Pantanowitz L. Multiplex Immunohistochemistry and Immunofluorescence: A Practical Update for Pathologists. Mod Pathol. 2023 Jul;36(7):100197. doi: 10.1016/j.modpat.2023.100197. Epub 2023 Apr 25. PMID: 37105494.
Enkilife mIF 技术服务
-
提供有偿代检和分析服务
-
承接多色配套服务