抗体纯化用哪种?常用方法大盘点,一看就懂
发表时间:2026-03-27
抗体纯化是指从血清中分离多克隆抗体,或从腹水液或杂交瘤细胞系的培养上清液中分离单克隆抗体的过程。其核心目标是获得高纯度、高活性且满足特定应用要求的抗体。
抗体纯化是依据抗体自身的生物学特性,如分子电荷、分子量大小、疏水性等,选择适配方法并通过多步层析技术,从复杂混合物中分离出目标抗体的过程。常用方法包括Protein A/G 亲和层析、离子交换层析、凝胶过滤层析、疏水作用层析等,可最终获得高纯度抗体。其中,亲和层析仅需一步快速捕获,通常就能满足纯度与产量要求;若需进一步去除杂质、精制抗体或其片段,可搭配其他方法深度纯化。具体纯化方案的选择,主要取决于抗体来源、实验周期、成本预算及最终应用场景。
1、辛酸-硫酸铵沉淀法
辛酸-硫酸铵沉淀法利用辛酸和硫酸铵的特性,选择性地沉淀和纯化抗体,主要用于从血清或腹水中提取IgG抗体。
在微酸性条件下,辛酸与血清或腹水中的其他蛋白质结合并使其沉淀,而IgG抗体则保留在上清液中。这是因为辛酸会破坏杂蛋白的水化膜,促使其析出,而 IgG 因自身结构特点,不易被辛酸沉淀。
经辛酸处理大部分杂蛋白后,再使用饱和硫酸铵进行盐析。硫酸铵与溶液中的抗体竞争水分子,降低抗体的溶解度,从而导致其沉淀。将等体积的饱和硫酸铵溶液缓慢加入中和后的抗体样品中,然后在室温或4°C下孵育数小时。离心并去除上清液后,抗体沉淀溶解在缓冲溶液中。
沉淀的选择性、产量、纯度和重现性取决于几个因素,包括时间、温度、pH值和盐的添加速率。硫酸铵沉淀可以为某些抗体应用提供足够的纯化效果;然而,在大多数情况下,它作为柱层析或其他纯化方法之前的初步纯化步骤。
2、亲和层析法
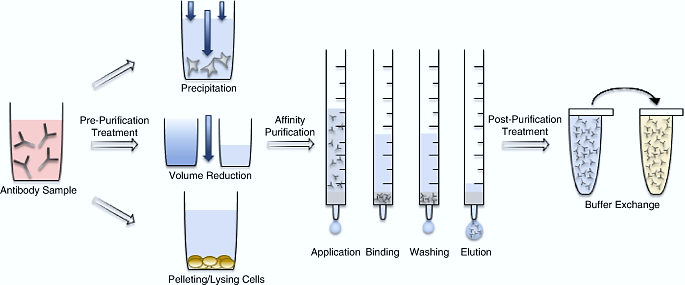
亲和层析是一种基于生物分子特异性相互识别的高效分离纯化技术。该方法将 Protein A、G、L 等特异性配体偶联于琼脂糖等固相载体上,构建出具备选择性吸附能力的分离体系。当复杂混合物上样后,配体可特异性捕获目标抗体,杂质则直接流穿,最终洗脱获得高纯度抗体,尤其适合从组分复杂、杂质远多于目标抗体的样品中分离抗体。
Protein A 能高效结合人、小鼠、兔、猪、犬等多种哺乳动物的 IgG,对人源 IgG1、IgG2、IgG4 亚型亲和力极高,但与 IgG3 结合较弱。相比之下,Protein G 对多数哺乳动物 IgG 的亲和力更强、结合谱更广,可有效结合人 IgG3、小鼠 IgG1、大鼠 IgG2a 等 Protein A 难以识别的抗体类型。重组 Protein G剔除了白蛋白结合位点与细胞表面结合位点,大幅降低非特异性吸附,显著提升抗体纯度,已成为纯化无法与 Protein A 高效结合的哺乳动物单克隆 / 多克隆 IgG 的重要工具。
Protein L 依靠其 N 端的 5 个同源结构域,可特异性结合抗体的κ 轻链,能够捕获含 κ 轻链的各类抗体分子,涵盖 IgG、IgM、IgA、IgE、IgD 等完整抗体,以及 ScFv、Fab 等抗体片段。它对人、小鼠、大鼠、兔来源的抗体结合效果良好,但不结合山羊、绵羊免疫球蛋白。Protein L为特殊结构抗体的纯化提供了关键解决方案。
3、抗原亲和纯化法
抗原亲和纯化是一种基于抗原?抗体特异性识别的高效抗体纯化技术。该方法以目标抗原作为亲和配体,通过化学偶联将其固定在凝胶介质上,构建出高选择性的亲和层析体系;样品中的目的抗体会与抗原发生特异性结合,经洗脱后即可获得高纯度抗体。与 Protein A/G 等传统 Fc 区结合纯化法不同,抗原亲和纯化直接靶向抗体可变区,可实现针对特定抗原表位抗体的精准捕获。抗原亲和纯化的核心优势在于特异性极高,尤其适合从多克隆抗体混合物中分离抗原特异性抗体。由于需要以大量高纯度抗原作为配体,该方法通常需要提前合成或纯化目标抗原。相较于常规 Fc 区结合法,抗原亲和纯化的选择性更突出,由此获得的抗体兼具高灵敏度与高特异性,非常适用于免疫组化(IHC)、免疫荧光(IF)等免疫学检测实验,即使在较低稀释倍数下使用,也不会升高背景信号。
4、离子交换层析法
离子交换层析依据蛋白质在特定缓冲体系中的净电荷差异进行分离,利用带正电或负电的层析树脂与蛋白结合。抗体属于蛋白质,由两性电解质氨基酸构成,其侧链上的酸性 / 碱性基团可在特定 pH 缓冲液中发生电离,使分子整体带电。等电点(pI)是离子交换层析条件选择的核心依据,该方法按固定相电荷性质分为阴离子交换层析和阳离子交换层析两类。
当抗体处于低于其等电点的pH环境中时,它们主要发生碱性解离,以带正电荷的阳离子状态存在,可与阳离子交换剂结合。相反,当抗体处于高于其等电点的pH环境中时,它们主要发生酸性解离,以带负电荷的阴离子状态存在,可与阴离子交换剂结合。由于待分离物质与离子交换基团的亲和力不同,通过逐步调节缓冲液的 pH 与离子强度,即可实现抗体与杂质的有效分离。
5、疏水相互作用层析法
疏水相互作用层析(HIC)是一种基于样品分子的疏水基团与色谱介质的疏水配体在盐水系统中疏水作用力差异实现分离的色谱技术。单克隆抗体在其分子结构中包含众多非极性氨基酸。这些非极性氨基酸的侧链暴露在抗体分子表面,可聚集在一起形成疏水区域,在稳定抗体的三级和四级结构中发挥作用。不同单克隆抗体之间的疏水区域强度存在显著差异。
随着溶液中盐浓度的增加,疏水相互作用增强。因此,大多数疏水相互作用层析过程涉及在高盐浓度条件下上样,并在低盐浓度条件下进行洗脱。疏水作用层析介质的核心特点是疏水性较弱,与蛋白质的相互作用温和,因此能最大程度维持生物大分子的天然构象与生物活性。同时,疏水作用层析还擅长从大体积样品中富集低丰度的目标蛋白。
6、凝胶过滤层析法
凝胶过滤层析法,又称尺寸排阻层析或分子筛层析,是抗体纯化中依据分子大小差异实现分离的常用技术。该方法以多孔凝胶颗粒作为固定相,让溶液中的分子按尺寸大小实现分离。当样品流经层析柱时,分子量较大的抗体无法进入凝胶孔隙,会被快速洗脱;而小分子杂质可进入凝胶内部,迁移速度更慢、洗脱滞后,借此实现抗体与杂质的有效分离。该方法分辨率虽低于亲和层析等特异性纯化技术,但具备操作简便、条件温和、适用范围广等优势。

生物亲和配体Protein-A、-G、-L和-M概述
| 蛋白质类型 | 结合对象 | 优势 | 劣势 |
|---|---|---|---|
| Protein A |
?IgG、IgG片段和亚类(除IgG3外),IgG Fc区域上连接CH2和CH3的铰链区(高亲和力~10 nM) ?Fc融合蛋白 ?IgM和IgE |
?高流速 ?高结合量 ?可结合IgG的Fc、Fab以及F(ab’)?片段 |
?存在一些与宿主细胞蛋白的非特异性结合 |
| Protein G |
?IgG1、IgG2、IgG3、IgG4 ?IgG Fc区域上CH2 与 CH3 之间的铰链区(高亲和力~10 nM) ?通过 CH1 结构域结合 Fab 段恒定区(低亲和力,μΜ级) ?人源IgE、IgD和IgA |
?对IgG的结合谱比Protein A更广 |
?对严苛洗脱条件的耐受性弱于 Protein A |
| Protein L |
?κ轻链的可变区(KD ~ 100 mM),可结合IgG、IgM、IgA、IgE和IgD |
?在腹水或细胞培养上清中结合抗体效率极高 ?对 IgM 结合效果非常好 |
?不适用于多克隆抗体纯化 |
| Protein M |
?抗体轻链VL与Vκ的保守区域(FR) |
?可广谱识别并结合多种类型的抗体 |
|
总结:怎么选最适合你的方法?
-
追求低成本、快速粗提:选辛酸硫酸铵沉淀
-
常规科研抗体:首选 Protein A/G 亲和层析
-
特殊抗体 / 无 Fc 段抗体:用 Protein L
-
高特异性诊断抗体:用抗原亲和纯化
-
精细除杂、保活性:搭配离子交换 + 疏水层析
-
脱盐、换液、除聚合体:凝胶过滤层析
抗体纯化没有单一万能方法,多级组合、由粗到精,才能稳定获得高纯度、高活性、适配场景的优质抗体。
EnkiLife推出的重组兔单克隆抗体 为科研需求提供高效解决方案,拥有超过 7,000 种的丰富产品组合,完全兼容多样化的实验场景。访问查看:
https://www.enkilife.cn/product/index?action=search&cate=94




