文献分享:锰暴露通过 cGAS-STING/ROS 调控细胞凋亡与铁死亡
发表时间:2026-03-31一、研究背景
锰(Mn)是人类和哺乳动物必需的微量元素,广泛参与体内多种生理过程,包括骨骼形成、能量代谢、神经递质合成及免疫功能调节,对维持机体正常生理运转具有不可替代的作用。然而,随着工业化进程的快速推进,锰矿开采、冶金冶炼、电池生产等行业的规模化发展,导致环境中锰的暴露水平逐年升高,职业暴露与环境暴露引发的锰中毒事件频发,其环境毒性风险已成为全球关注的公共卫生热点问题。其中,锰暴露所致的神经毒性尤为突出,长期过量暴露会导致神经系统结构和功能损伤,引发类帕金森病、认知障碍、情绪异常等一系列神经退行性病变,严重威胁人类健康,目前针对锰神经毒性的防控和治疗仍缺乏有效的靶点和手段,其潜在分子机制亟待深入解析。
已有研究表明,锰具有丰富的免疫调节功能,能够调控先天免疫和适应性免疫反应,而cGAS-STING通路作为先天免疫体系中的核心通路,在识别胞质DNA、启动抗病毒免疫反应、调控炎症因子释放及细胞命运决定中发挥关键作用。近年来,越来越多的研究发现,cGAS-STING通路的异常激活与多种神经退行性疾病、氧化应激损伤及细胞凋亡密切相关,但截至目前,关于cGAS-STING通路在锰暴露诱导神经毒性中的具体作用、调控规律,以及其与氧化应激、细胞凋亡、铁死亡等损伤机制之间的关联,尚未明确阐明,这也成为当前锰神经毒性研究领域的重要空白。
为此,Zhang等人在《Redox Biology》发表了题为《Mn exposure mediates ROS generation and further induces apoptosis and ferroptosis through activation of the cGAS–STING pathway》的研究论文,针对上述研究缺口,采用体内外实验相结合的方式,以BV2小胶质细胞和小鼠为研究模型,系统探究锰暴露对cGAS-STING通路的调控作用,以及该通路与ROS、细胞凋亡、铁死亡之间的内在关联,深入揭示锰暴露诱导神经毒性的潜在分子机制,为锰神经毒性相关疾病的防控、靶点筛选及临床干预提供了新的研究视角和坚实的理论依据。
二、研究方法
本研究采用BV2小胶质细胞与小鼠脑组织整合模型进行交叉验证,首先用不同浓度的MnCl?·4H?O处理BV2小胶质细胞构建细胞毒性模型,同时通过锰暴露处理小鼠构建体内模型。之后采用Western blot检测cGAS、STING等相关蛋白的表达水平,DCFH-DA荧光探针结合流式细胞术和荧光酶标仪检测细胞内ROS水平,生化试剂盒检测GSH-Px、SOD活性及MDA、Fe2?含量,JC-1染色结合流式细胞术检测线粒体膜电位,Annexin V-FITC/PI双染色检测细胞凋亡率,透射电镜观察小鼠海马体线粒体超微结构,免疫荧光检测脑组织中ACSL4的表达,RNA-seq筛选差异表达基因,同时构建cGAS?/?和STING?/? BV2细胞系,以及采用ROS抑制剂共处理,探究cGAS-STING通路、ROS与细胞凋亡、铁死亡之间的调控关系。所有实验均重复3-5次,采用SPSS 26.0软件进行统计分析,Graphpad Prism 9软件绘制图表,P<0.05为差异具有统计学意义。
三、重点结果分析
体外核心基础:锰暴露激活cGAS-STING通路并引发细胞氧化应激
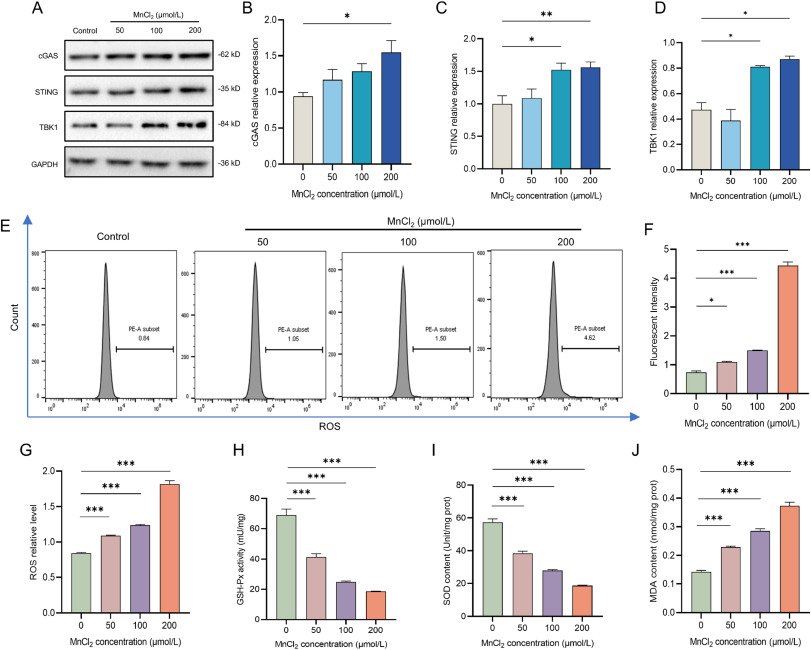
作为整个研究体外实验的起点,研究者首先以BV2小胶质细胞为研究对象,探究锰暴露对细胞内关键通路及氧化状态的影响,为后续机制解析筑牢基础。研究者用不同浓度的氯化锰处理细胞后,通过蛋白印迹检测发现,随着处理浓度的梯度升高,细胞内cGAS、STING及TBK1三种关键蛋白的表达水平也呈浓度依赖性显著上升,且所有差异均达到统计学显著标准,这一结果清晰证实,锰暴露能够特异性激活小胶质细胞中的cGAS-STING通路,且这种激活效应与锰暴露剂量密切相关。在此基础上,进一步通过荧光探针结合流式细胞术检测细胞内活性氧水平,同时检测抗氧化酶活性及脂质过氧化标志物含量,结果发现,锰处理后细胞内活性氧荧光强度显著增强,抗氧化系统中的GSH-Px和SOD活性明显下降,而脂质过氧化产物MDA的含量则持续升高,这意味着锰在激活cGAS-STING通路的同时,会同步引发细胞的氧化应激反应,二者相互关联、协同作用,共同构成锰诱导细胞损伤的初始环节。
体内实验验证:锰暴露的神经毒性及通路激活效应在动物体内的重现
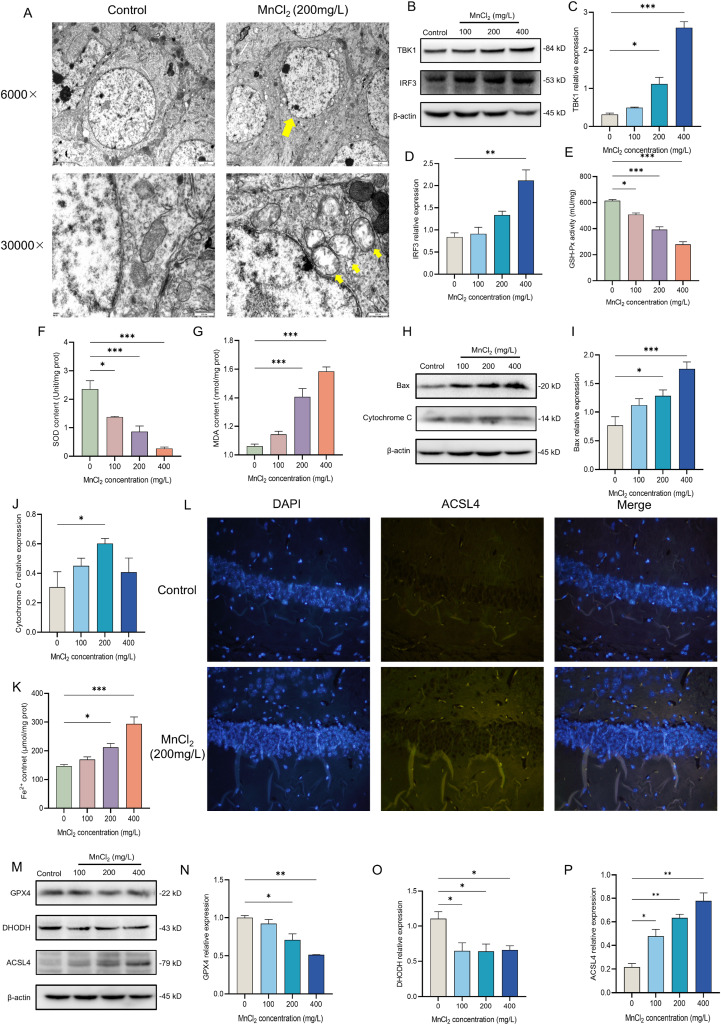
为了验证体外实验结果的可靠性,同时明确锰暴露在体内的神经毒性效应,研究者构建了锰暴露小鼠模型,以小鼠海马体为核心研究部位,开展体内验证实验。通过透射电镜观察发现,经锰处理后的小鼠海马体细胞出现明显的结构损伤,细胞膜发生皱缩,线粒体作为细胞能量代谢的核心,出现基质肿胀、空泡化、嵴缩短等典型损伤特征,直观展现了锰暴露对神经组织的直接损伤作用。进一步通过蛋白印迹检测小鼠脑组织中的通路相关蛋白,结果与体外实验高度一致,随着锰暴露浓度的升高,脑组织中TBK1和IRF3的表达水平显著上升,证实cGAS-STING通路在体内同样会被锰暴露激活。除此之外,研究者还检测了脑组织中氧化应激、凋亡及铁死亡相关指标,发现锰暴露会导致脑组织中抗氧化酶活性下降、脂质过氧化产物积累,同时促凋亡蛋白和铁死亡促进蛋白表达升高,抑制性蛋白表达降低,铁离子含量也显著增加,这一系列结果与体外实验形成完美呼应,充分证实锰暴露在体内可通过激活cGAS-STING通路,诱导氧化应激、细胞凋亡和铁死亡,进一步夯实了研究结论的科学性和可靠性。
核心机制解析:ROS在通路与细胞损伤之间的介导作用
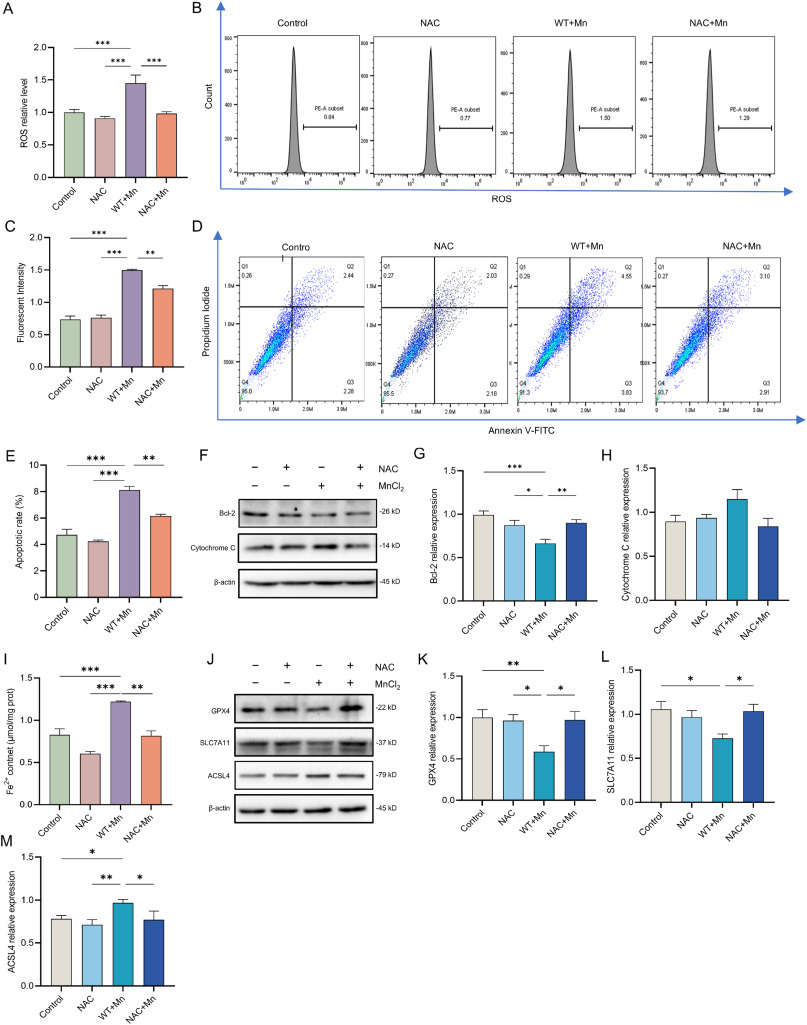
明确了锰暴露可激活cGAS-STING通路并诱导细胞凋亡、铁死亡后,研究者进一步探究三者之间的核心调控关系,重点验证ROS是否发挥介导作用。研究者采用ROS抑制剂NAC与锰共处理BV2小胶质细胞,首先通过检测确认,NAC预处理能够有效降低锰诱导的细胞内ROS水平,证明NAC可成功阻断锰介导的ROS生成。在此基础上,对细胞凋亡情况进行检测,发现NAC预处理后,锰处理组的细胞凋亡率显著下降,同时抗凋亡蛋白Bcl-2的表达水平升高,促凋亡蛋白细胞色素C的表达水平降低,这一结果表明,抑制ROS生成能够有效减轻锰诱导的细胞凋亡。随后,研究者进一步检测铁死亡相关指标,发现NAC预处理同样能够降低锰处理组细胞内的铁离子含量,减少铁死亡促进蛋白ACSL4的表达,同时升高铁死亡抑制蛋白GPX4、SLC7A11的表达,证实抑制ROS也能缓解锰诱导的细胞铁死亡。综合以上实验结果,研究者明确了整个机制的核心逻辑:cGAS-STING通路被锰激活后,会介导ROS大量生成,而ROS作为关键介导分子,进一步诱导细胞发生凋亡和铁死亡,成为连接通路激活与细胞损伤的核心纽带。
机制总结:锰暴露诱导神经毒性的完整调控网络
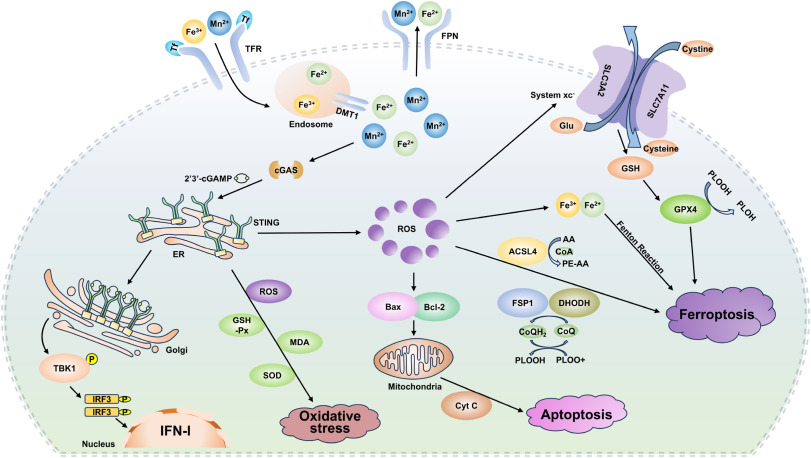
基于上述所有体外和体内实验结果,研究者绘制了锰暴露诱导神经毒性的完整机制示意图,将所有关键调控环节整合为一个连贯的调控网络,清晰呈现了锰诱导神经毒性的全过程。整个调控过程以锰暴露为起始信号,首先刺激细胞内cGAS合成第二信使cGAMP,cGAMP进一步结合并激活STING蛋白,激活后的STING会推动下游TBK1和IRF3的磷酸化,进而促进I型干扰素的表达。与此同时,被激活的cGAS-STING通路会引发明显的氧化应激反应,具体表现为ROS和MDA等氧化产物的大量生成,以及GSH-Px、SOD等抗氧化酶活性的下降。而ROS作为核心介导分子,会进一步启动两条损伤通路:一方面通过调控Bax、Bcl-2等凋亡相关蛋白的表达,诱导线粒体释放细胞色素C,最终引发细胞凋亡;另一方面通过破坏细胞内铁稳态,调控GPX4、SLC7A11、ACSL4等铁死亡关键蛋白的表达,进而诱导细胞发生铁死亡。这一完整的调控网络,将cGAS-STING通路、ROS、凋亡和铁死亡有机串联,清晰阐明了锰暴露诱导神经毒性的核心机制,也浓缩了整个研究的核心结论。
四、结论
本研究通过体内外实验证实,Mn暴露可激活cGAS-STING通路,介导ROS生成,进而诱导BV2小胶质细胞和小鼠脑组织细胞发生凋亡和铁死亡,这是Mn神经毒性的关键机制。研究不仅填补了cGAS-STING通路在Mn神经毒性中作用的研究空白,还明确了ROS在cGAS-STING通路与凋亡、铁死亡之间的介导作用,为Mn神经毒性相关疾病的防控提供了新的靶点和思路。未来可进一步深入探究cGAS-STING通路与ROS相互作用的具体分子机制,同时通过抑制剂或基因敲除小鼠模型进行体内验证,并结合人群样本数据,为Mn神经毒性的临床干预提供更坚实的理论和实验支持。
参考文献
Zhang Z, Yang J, Zhou Q, Zhong S, Luo J, Chai X, Liu J, Zhang X, Chang X, Wang H. The role and mechanism of the cGAS-STING pathway-mediated ROS in apoptosis and ferroptosis induced by manganese exposure. Redox Biol. 2025 Sep;85:103761. doi: 10.1016/j.redox.2025.103761. Epub 2025 Jul 8. PMID: 40652697; PMCID: PMC12274772.
2h 极速 WB 即用型全流程试剂盒