淫羊藿素新用:抑制中性粒细胞陷阱,狙击尿路上皮癌
发表时间:2026-04-03
一、研究背景
尿路上皮癌是泌尿系统最常见的恶性肿瘤之一,肿瘤复发和转移是导致患者死亡的主要原因,尽管铂类化疗、PD1抗体免疫治疗等新疗法已应用于临床,但仍有超过一半的患者对这些治疗无响应,因此寻找新型治疗药物和治疗靶点成为改善尿路上皮癌患者预后的迫切需求。
淫羊藿素(Icaritin, ICT)作为传统中药淫羊藿的主要活性成分淫羊藿苷(Icariin, ICA)的体内代谢产物,是近年来肿瘤研究领域的热点分子。2022 年,以 ICT 为核心成分的淫羊藿素胶囊获中国国家药品监督管理局批准,用于晚期不可切除肝细胞癌的一线治疗,其在延长肝细胞癌患者总生存期方面展现出显著疗效。现有研究已证实,ICT 兼具直接抗肿瘤与免疫调控双重作用:既能通过诱导肿瘤细胞凋亡、自噬等方式直接杀伤肿瘤细胞,又能重塑肿瘤免疫微环境,激活机体抗肿瘤免疫反应。然而,相较于其在肝细胞癌中的深入研究,ICT 在尿路上皮癌中的具体作用机制,尤其是其对肿瘤免疫微环境的调控规律,目前尚未得到系统阐明,这也成为限制其在尿路上皮癌临床转化的关键因素。
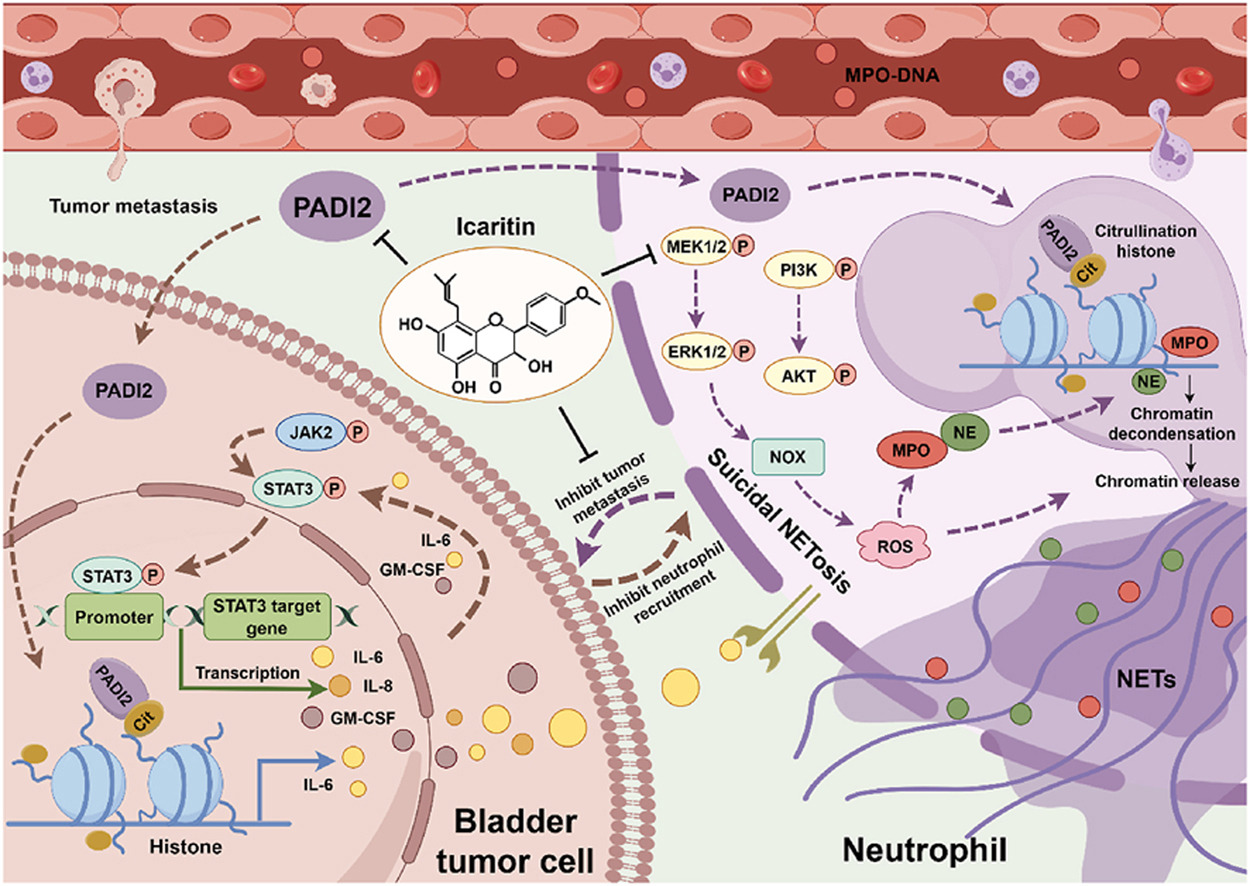
在肿瘤微环境中,负调控分子和多种免疫细胞亚群会抑制抗肿瘤免疫,其中中性粒细胞及其产生的中性粒细胞胞外陷阱(NETs)所构建的炎症微环境,被证实会促进肿瘤转移,然而目前尚无专门针对中性粒细胞和NETs的特异性抑制药物。在此背景下,研究性论文《Icaritin inhibits the progression of urothelial cancer by suppressing PADI2-mediated neutrophil infiltration and neutrophil extracellular trap formation》,首次揭示了淫羊藿素在尿路上皮癌治疗中的潜在价值,通过深入探究其作用机制,为尿路上皮癌的治疗提供了新的思路和靶点。
二、研究方法
本研究综合运用体外细胞实验、体内动物模型和临床样本分析等多种研究方法,首先采用人尿路上皮癌细胞系(UMUC-3、T24)和小鼠尿路上皮癌细胞系(MB49)进行体外实验,通过CCK-8法检测ICT对肿瘤细胞活力的影响,借助划痕实验、Transwell实验评估肿瘤细胞迁移和侵袭能力,利用流式细胞术分析细胞凋亡和周期变化,同时通过中性粒细胞分离、NETs生成实验探究ICT对中性粒细胞及NETs的调控作用;体内实验构建了小鼠皮下肿瘤模型、原位尿路上皮癌模型和尾静脉肺转移模型,通过灌胃给予不同剂量ICT,观察肿瘤生长和转移情况,结合流式细胞术、免疫组化等方法分析肿瘤微环境中免疫细胞的浸润变化;临床研究方面,收集了195例石蜡包埋尿路上皮癌样本、24例新鲜肿瘤样本和40例血清样本,通过免疫组化、ELISA、回顾性分析等方式,探究中性粒细胞、NETs与尿路上皮癌预后及免疫逃逸的相关性,此外还通过Western blot、RT-qPCR、Biacore、分子对接等技术深入解析ICT的作用机制,所有实验数据均采用GraphPad Prism和R软件进行统计学分析。
三、结果分析
1. ICT在体内通过抑制中性粒细胞浸润来抑制肿瘤转移
研究首先从体外实验入手,探究ICT对尿路上皮癌细胞恶性生物学行为的影响。通过不同浓度ICT处理UMUC-3、T24、MB49三种尿路上皮癌细胞系,明确其半数抑制浓度(IC??)分别为15.71、19.55和9.32 μmol/L,且 ICT 对肿瘤细胞活力和集落形成的抑制作用呈浓度依赖性,同时诱导细胞凋亡、阻滞细胞周期,初步证实了ICT的抗肿瘤潜力。但ICT对肿瘤细胞迁移侵袭抑制效果不显著,为后续探究其通过肿瘤微环境发挥作用提供了重要线索。
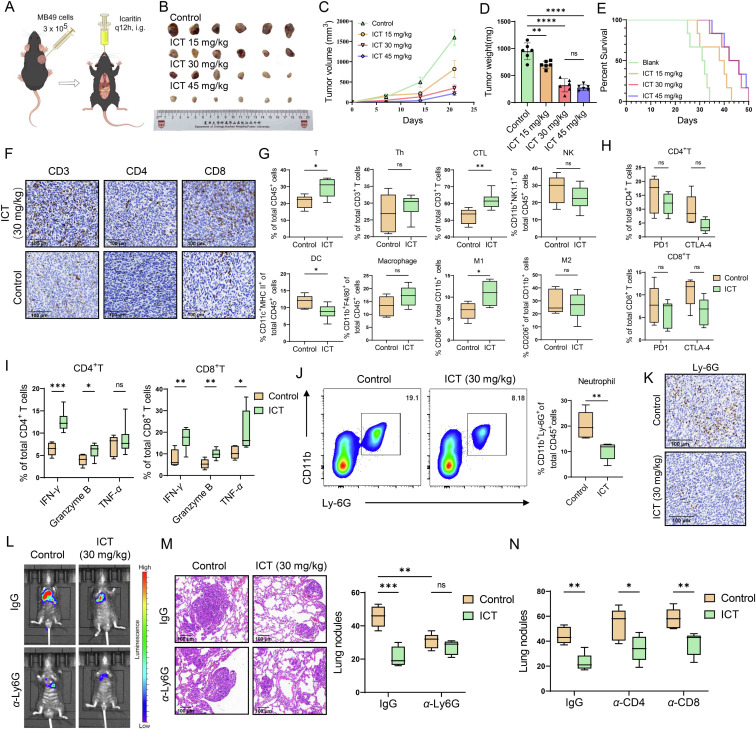
之后的实验明确了ICT体内抗肿瘤的核心机制的关键靶点——中性粒细胞,研究者首先构建小鼠皮下肿瘤模型,设置对照组和低、中、高三个ICT剂量组,连续灌胃21天后,通过游标卡尺每周测量肿瘤体积、称量肿瘤重量,发现ICT对肿瘤生长的抑制作用呈明显剂量依赖性,其中30 mg/kg剂量组肿瘤抑制率最高,且通过检测小鼠血清中谷丙转氨酶(ALT)、谷草转氨酶(AST)水平及小鼠体重变化,证实该剂量下ICT无明显肝毒性和全身不良反应,安全性良好,同时能显著延长小鼠生存期,为后续实验剂量选择提供了可靠依据。通过分析肿瘤免疫微环境发现,ICT 可促进细胞毒性 T 细胞、M1 型巨噬细胞的浸润及抗肿瘤免疫效应分子的分泌,同时使 PD-1、CTLA-4 等免疫检查点分子和 M2 型巨噬细胞水平呈下降趋势,该调控效果在小鼠肝癌皮下模型中也得到验证,且 ICT 能显著抑制肿瘤组织中中性粒细胞的浸润。进一步构建小鼠原位尿路上皮癌模型,证实 ICT 可抑制肿瘤生长,其对肿瘤微环境的调控作用与皮下模型基本一致,且对免疫检查点的抑制作用更显著。最关键的是在尾静脉注射MB49细胞构建肺转移模型后,ICT处理组小鼠肺转移灶数量显著少于对照组,HE染色结果显示转移灶面积明显缩小;而当耗尽小鼠体内中性粒细胞后,ICT的肺转移抑制作用减弱,肺转移灶数量恢复至接近对照组水平;反观单独耗尽CD4?或CD8?T细胞时,ICT仍能有效抑制肿瘤转移,这一对比实验清晰排除了T细胞的核心作用,明确证实中性粒细胞是ICT发挥体内抗肿瘤、抗转移作用的关键靶点,为后续聚焦中性粒细胞及NETs的研究奠定了核心基础。
2. 深度解析 ICT 抑制 NETs 形成的核心机制
NETs作为中性粒细胞发生 NETosis 后的产物,是介导肿瘤免疫微环境形成免疫抑制的关键因素,为此研究进一步探究了 ICT 对 NETs 形成的调控作用。通过免疫荧光染色(MPO和H3CIT双标)观察到,ICT处理后肿瘤组织中NETs形成显著减少。体外共培养实验中,PMA诱导的NETs可显著促进肿瘤细胞侵袭转移,而ICT能剂量依赖性逆转该效应,与DNase I联合使用时抑制效果更显著。体内实验进一步证实,ICT可减少肺转移灶中NETs形成,同时抑制肿瘤EMT转化和肿瘤干细胞特性。
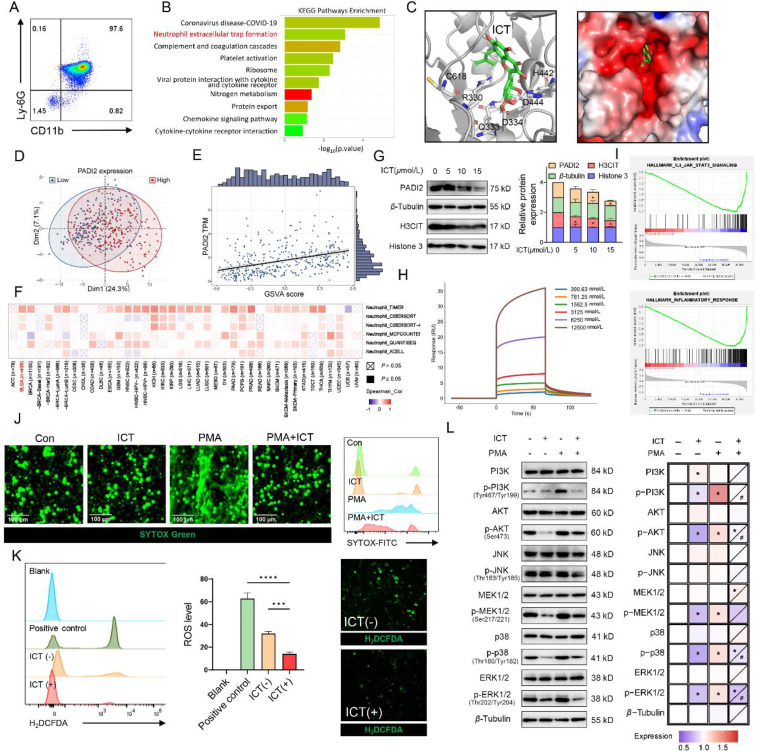
为解析 ICT 抑制 NETs 形成的核心分子机制,研究首先分离出 CD45+CD11b+中性粒细胞,经 ICT 处理后进行 RNA 测序及功能富集分析,发现 ICT 可调控与 NETs 形成、趋化因子信号相关的通路,且差异基因分析显示,与组蛋白瓜氨酸化和 NETs 形成密切相关的 PADI2 基因表达被显著下调。分子对接实验结果提示,ICT 可与 PADI2 蛋白的 6 个潜在位点相结合;同时结合尿路上皮癌中 PADI2 表达与中性粒细胞浸润的相关性分析、基因集变异分析结果,研究提出 ICT 调控 NETs 形成可能依赖 PADI2 的假说。后续蛋白质印迹实验为该假说提供了关键证据,结果显示 ICT 可呈浓度依赖性降低 PADI2 及其下游靶点 H3CIT 的蛋白表达,而 Biacore 表面等离子体共振实验进一步证实,ICT 与 PADI2 之间存在直接的相互作用。考虑到 PMA 诱导的自杀性 NETosis 是肿瘤微环境中 NETs 形成的主要方式,研究进一步验证了 ICT 对该过程的调控作用,发现 ICT 可有效抑制中性粒细胞的自杀性 NETosis,同时显著减少该过程中标志性的活性氧生成,且高浓度 ICT 还能下调 NETs 中 MMP9、VEGFA、HMGB1 等促肿瘤转移相关蛋白的表达。结合基因集富集分析及通路验证结果,研究还揭示 ICT 可抑制 MAPK 信号通路的激活,其中对 PI3K/AKT 通路、MEK/ERK/p38 通路的抑制作用显著,而对 JNK 通路无明显调控效果。综上,研究明确了 ICT 抑制 NETs 形成的双重分子路径:一方面直接结合并抑制 PADI2 活性,阻断其介导的组蛋白瓜氨酸化;另一方面抑制 ROS 生成与 MAPK 信号通路激活,从而抑制中性粒细胞的自杀性 NETosis,这一发现为阐释 ICT 的抗肿瘤作用机制提供了全新的视角。
3. PADI2 介导 NETs 对尿路上皮癌具有预后价值
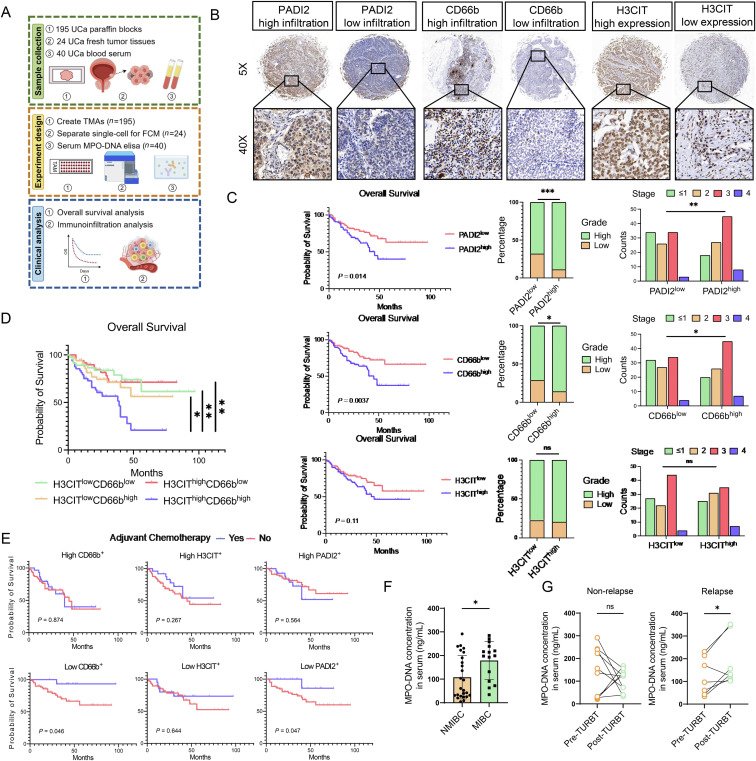
为验证 PADI2 介导的 NETs 能否作为尿路上皮癌的预后生物标志物,研究收集了尿路上皮癌患者的肿瘤组织与血液样本开展相关性分析,并对样本中 PADI2、中性粒细胞标志物 CD66b 及 NETs 标志物 H3CIT 进行了免疫组化检测。通过对 195 例可评估患者的回顾性分析发现,肿瘤组织中 CD66b 高表达与患者不良临床预后相关,且 CD66b 表达水平还与肿瘤高分级、病理晚期密切关联,而 H3CIT 的单独表达未表现出该相关性,推测这一现象可能与 H3CIT 在肿瘤组织中存在固有表达有关。对 CD66b 与 H3CIT 进行联合分析后发现,两种标志物均高表达的患者预后最差。研究进一步分析中性粒细胞、NETs 与化疗敏感性的关联,结果显示肿瘤组织中的中性粒细胞浸润与患者的化疗耐药性相关。为明确 NETs 与肿瘤进展、复发的关系,研究对 40 例患者的外周血清进行 ELISA 检测,发现肌层浸润性膀胱癌患者的血清 MPO-DNA 水平显著高于非肌层浸润性膀胱癌患者;而对经尿道膀胱肿瘤电切术术后患者的随访结果显示,术后血浆 MPO-DNA 水平升高的患者更易出现肿瘤复发。上述研究结果充分证实,中性粒细胞及 NETs 相关成分具备预测尿路上皮癌复发与疾病进展的潜在价值,尽管 H3CIT 的单独表达并非可靠的尿路上皮癌预后指标,但将其与 CD66b 联合检测,可显著提升对肿瘤患者预后的预测效能。
4. ICT与抗PD-1协同发挥抗肿瘤作用
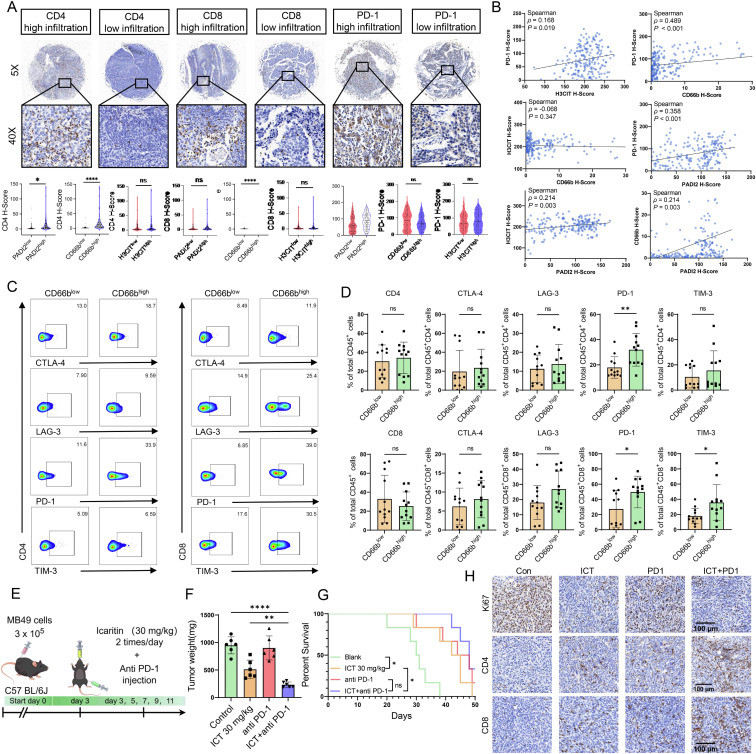
已有研究证实,肿瘤微环境中的中性粒细胞与 NETs 会抑制 T 细胞的抗肿瘤功能,诱导 T 细胞发生耗竭并最终导致肿瘤免疫逃逸,为此研究进一步分析了肿瘤组织中中性粒细胞、NETs 与 T 细胞耗竭三者间的关联。相关性分析结果显示,肿瘤内的中性粒细胞浸润、NETs 形成虽与 T 细胞浸润增加相关,但同时也会伴随 PD-1 表达的显著升高。研究收集 24 例尿路上皮癌患者的新鲜肿瘤组织,制备单细胞悬液后进行流式细胞术分析,发现肿瘤组织中 CD66b 阳性中性粒细胞的浸润程度与 PD-1、CD8+TIM3 的表达上调呈正相关,提示高中性粒细胞浸润与肿瘤免疫耗竭密切相关。在证实 ICT 可抑制中性粒细胞浸润与 NETs 形成的基础上,研究进一步探究了其与抗 PD-1 治疗联合应用逆转 T 细胞耗竭的效果,通过构建动物模型开展联合治疗实验发现,ICT 与抗 PD-1 治疗联用能显著抑制肿瘤生长,同时改善荷瘤小鼠的预后;对肿瘤组织的免疫组化分析显示,联合治疗组的 Ki67 表达显著降低,CD4+、CD8+T 细胞的浸润程度则明显升高。上述结果证实,ICT 可通过抑制中性粒细胞浸润与 NETs 形成实现肿瘤免疫微环境的重塑,进而逆转肿瘤免疫逃逸,而其与抗 PD-1 免疫治疗的联合应用能够产生协同效应,显著增强机体的抗肿瘤免疫作用。
四、结论
本研究首次系统揭示了ICT抑制尿路上皮癌进展的全新机制:ICT通过直接结合并抑制PADI2的表达,一方面抑制中性粒细胞的自杀性NETosis,减少NETs的形成,阻断NETs介导的肿瘤EMT和干细胞特性;另一方面抑制肿瘤细胞中PADI2介导的组蛋白瓜氨酸化,减少IL-6的转录和分泌,阻断IL-6/JAK2/STAT3正反馈循环,抑制中性粒细胞的招募,进而抑制肿瘤转移和进展。同时,临床研究证实中性粒细胞和NETs相关成分可作为尿路上皮癌的预后生物标志物,而ICT与抗PD-1免疫治疗的协同作用,为尿路上皮癌的临床治疗提供了新的策略。该研究不仅拓展了ICT的临床应用范围,填补了尿路上皮癌中NETs靶向治疗的空白,也为传统中药衍生物在肿瘤免疫治疗中的应用提供了新的理论依据。
参考文献
Mou Z, Chen Y, Hu J, Hu Y, Zou L, Chen X, Liu S, Yin Q, Gong J, Li S, Mao S, Xu C, Jiang H. Icaritin inhibits the progression of urothelial cancer by suppressing PADI2-mediated neutrophil infiltration and neutrophil extracellular trap formation. Acta Pharm Sin B. 2024 Sep;14(9):3916-3930. doi: 10.1016/j.apsb.2024.06.029. Epub 2024 Jul 1. PMID: 39309483; PMCID: PMC11413672.
2h极速WB即用型全流程试剂盒: