文献分享:TKI联合CTLA4阻断重塑肺腺癌脑转移免疫微环境的新机制
发表时间:2026-04-30一、研究背景
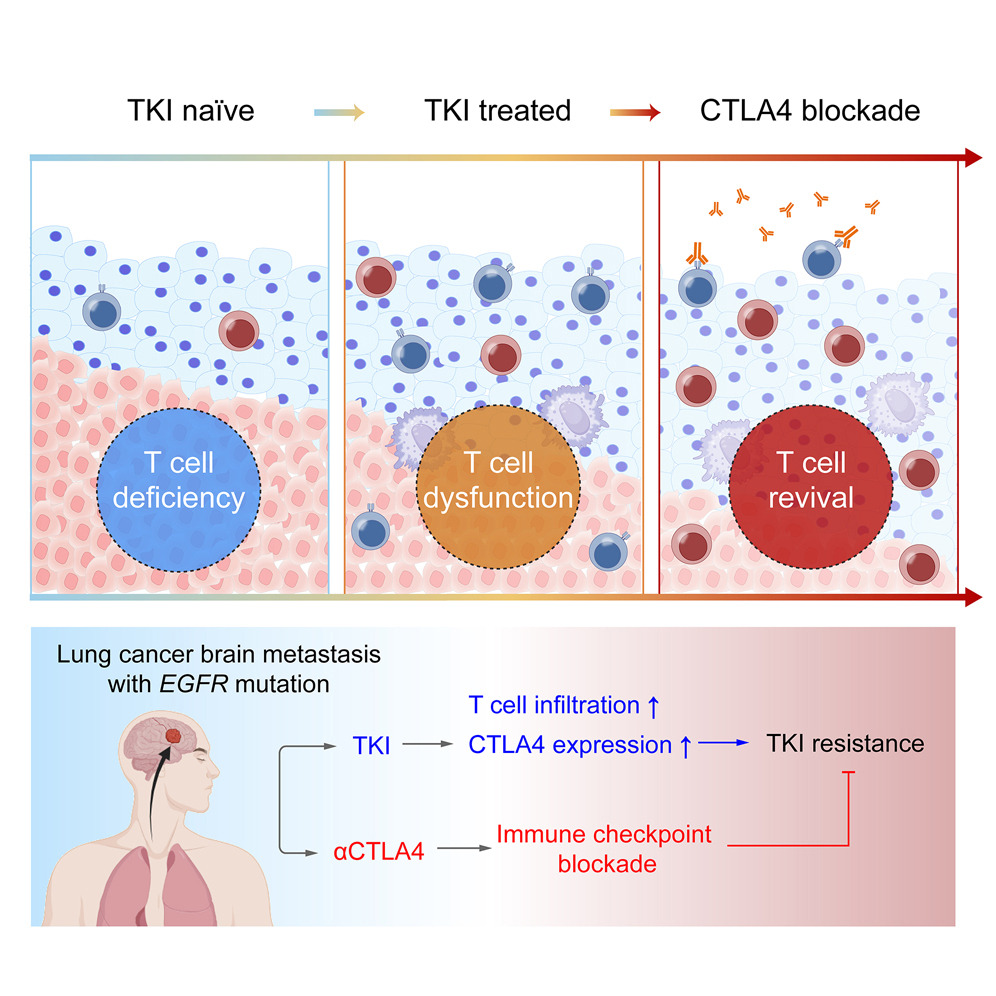
肺癌是全球癌症相关死亡的首要原因,约 40%–50% 的肺癌患者会出现中枢神经系统转移,而中枢神经系统内由脑驻留免疫细胞与浸润免疫细胞构成的转移微环境,打破了中枢神经系统为免疫豁免器官的传统认知,也直接决定了肺癌脑转移的进展与预后。尽管组织病理学诊断与影像学技术为认识肺癌脑转移提供了重要依据,但对全脑多样细胞网络的分子全景进行无偏解析,仍是全面理解疾病演进与生物学功能的关键。分子分型与靶向治疗的发展为特定基因变异患者带来显著收益,酪氨酸激酶抑制剂(TKI)的问世彻底改变了肺癌脑转移的治疗格局,尤其第三代 EGFR?TKI 奥希替尼可穿透血脑屏障,成为 EGFR 突变型肺癌脑转移的标准一线治疗。然而,TKI 获得性耐药仍是临床重大挑战,多数患者在治疗 1 年内出现疾病进展,耐药机制复杂多样,而免疫逃逸是其中关键驱动因素,提示激活抗肿瘤免疫应答有望克服 TKI 耐药。免疫检查点抑制剂已在多种肿瘤中证实临床价值,部分研究也提示靶向治疗与免疫治疗存在联合潜力,但免疫检查点阻断在 EGFR 突变型肺癌脑转移中的疗效仍十分有限,这也凸显了深入解析 TKI 诱导的肿瘤微环境重编程机制的迫切性。为此,相关学者在《Cancer Cell》发表了题为《Overcoming tyrosine kinase inhibitor resistance in lung cancer brain metastasis with CTLA4 blockade》的研究,旨在通过单细胞转录组测序与多重免疫组化,系统解析不同遗传背景与 TKI 治疗状态下肺癌脑转移的免疫微环境,证实 CTLA4 是克服 TKI 耐药的关键靶点,并在 EGFR 敏感及耐药突变的肺癌脑转移小鼠模型中证明,序贯使用 EGFR?TKI 与 CTLA4 阻断剂的疗效显著优于 TKI 单药或 TKI 联合 PD?1 阻断,为解决肺癌脑转移 TKI 耐药提供了全新的治疗策略。
二、研究方法
本研究整合了临床样本分析、细胞实验、动物模型验证及多组学技术,首先收集了31例EGFR突变型肺癌脑转移(LCBM)患者的新鲜样本和196例福尔马林固定石蜡包埋(FFPE)样本,对新鲜样本进行单细胞悬液制备、染色、分选后,采用单细胞RNA测序(scRNA-seq)技术,对TKI治疗前后的免疫细胞及肿瘤细胞进行高通量测序,通过无监督聚类分析解析细胞亚群组成,利用差异基因表达分析筛选TKI调控的关键基因及信号通路,明确免疫微环境的动态变化。分子水平验证方面,利用多色免疫组化(mIHC)技术检测FFPE样本中CD3E、CD8A、FOXP3、CTLA4等关键分子的蛋白表达及细胞定位,结合图像分析软件量化阳性细胞比例。采用免疫荧光(IF)技术观察HMGB1的核质分布的变化;通过Western blot技术检测NF-κB信号通路相关蛋白及CTLA4的表达水平;利用ELISA技术定量检测细胞培养上清液中HMGB1及趋化因子的含量,验证关键分子的表达差异。之后构建携带EGFR-L860R、EGFR-19del及EGFR-T790M突变的LCBM小鼠模型,结合氯膦酸脂质体耗竭单核细胞来源巨噬细胞、CUT&Tag测序、T细胞迁移实验等,探究TKI调控免疫微环境的分子机制。最后通过小鼠体内治疗实验,验证TKI联合CTLA4阻断剂的治疗效果及安全性,同时利用流式细胞术、时序scRNA-seq等追踪免疫微环境的动态变化。
三、结果分析
1、TKI重塑T细胞分化命运,诱导CTLA4介导的免疫抑制
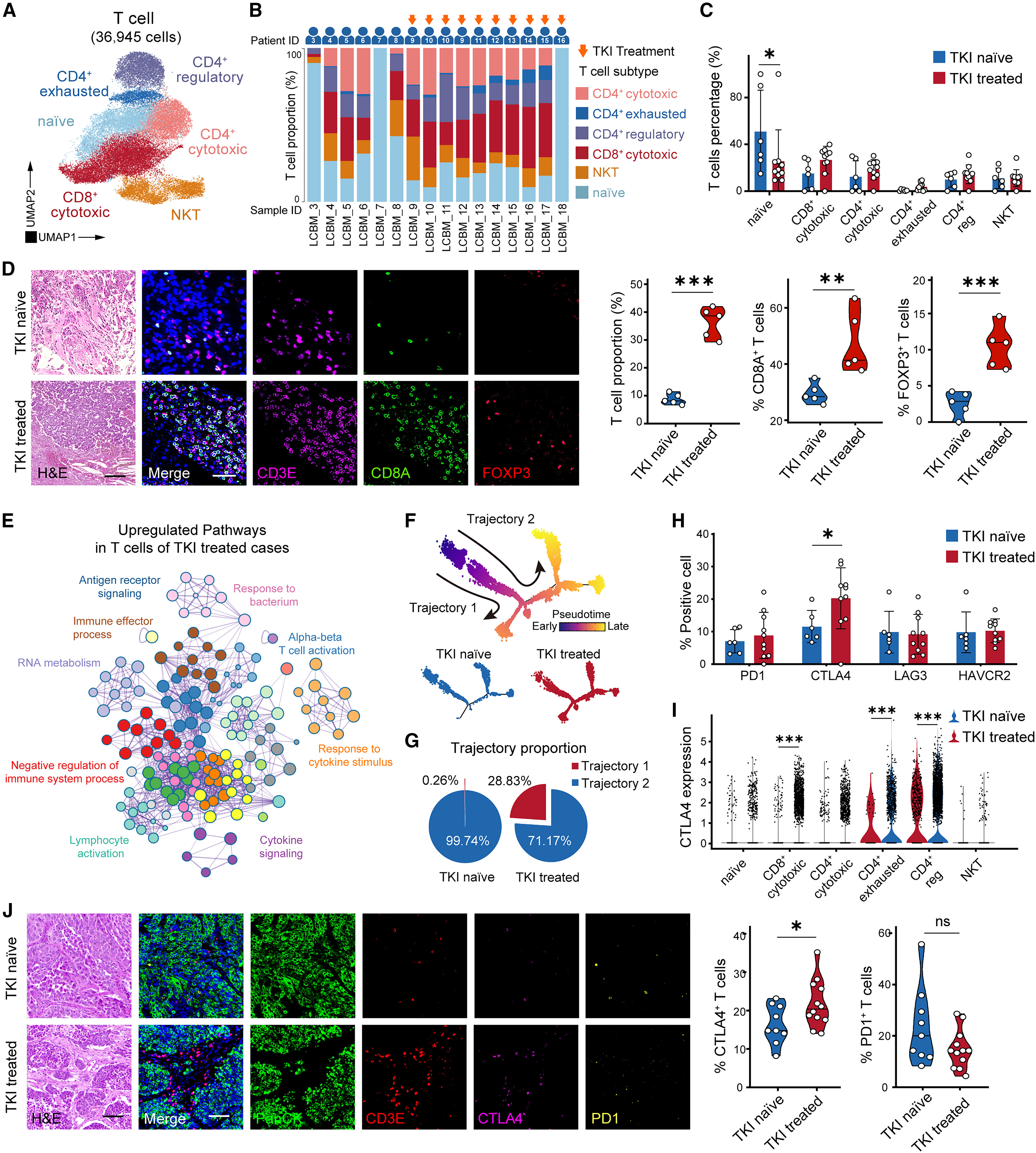
研究首先通过单细胞测序对TKI治疗前后的T细胞进行分群分析,发现T细胞可分为6个亚群,TKI治疗后T细胞的整体浸润水平显著升高,其中CD8+细胞毒性T细胞和CD4+调节性T细胞的比例均明显增加,且高浸润的CD8+细胞毒性T细胞可预测患者更好的预后,而初始T细胞和Tregs与预后无显著关联。更关键的是,TKI治疗显著改善了LCBM患者的预后,但这种治疗益处被同时出现的免疫抑制现象所抵消——差异基因表达分析显示,TKI治疗后T细胞中与淋巴细胞活化、细胞因子信号相关的通路被扰动,同时免疫检查点分子CTLA4被显著上调,而PD1、TIM3、LAG3等其他免疫检查点分子无明显变化。
进一步通过轨迹分析发现,T细胞存在两条发育轨迹(图F),TKI治疗组中28.83%的T细胞归属于轨迹1,而未接受TKI治疗组仅0.26%的T细胞属于该轨迹,且轨迹1后期CTLA4的表达水平显著升高,提示TKI诱导T细胞向表达CTLA4的免疫抑制表型分化。多色免疫组化验证显示,TKI治疗后CTLA4蛋白水平显著升高,且主要表达于CD8+细胞毒性T细胞、CD4+ Tregs和CD4+耗竭T细胞中,这三个亚群的CTLA4表达均在TKI治疗后显著上调,说明TKI对CTLA4的调控不具有亚群特异性。这些结果共同揭示,TKIs 在逆转 EGFR 突变型肺癌脑转移中 T 细胞缺乏的同时,也会通过上调 CTLA4 的表达削弱 T 细胞的效应功能。
2、TKI 治疗后单核细胞来源巨噬细胞介导 T 细胞招募
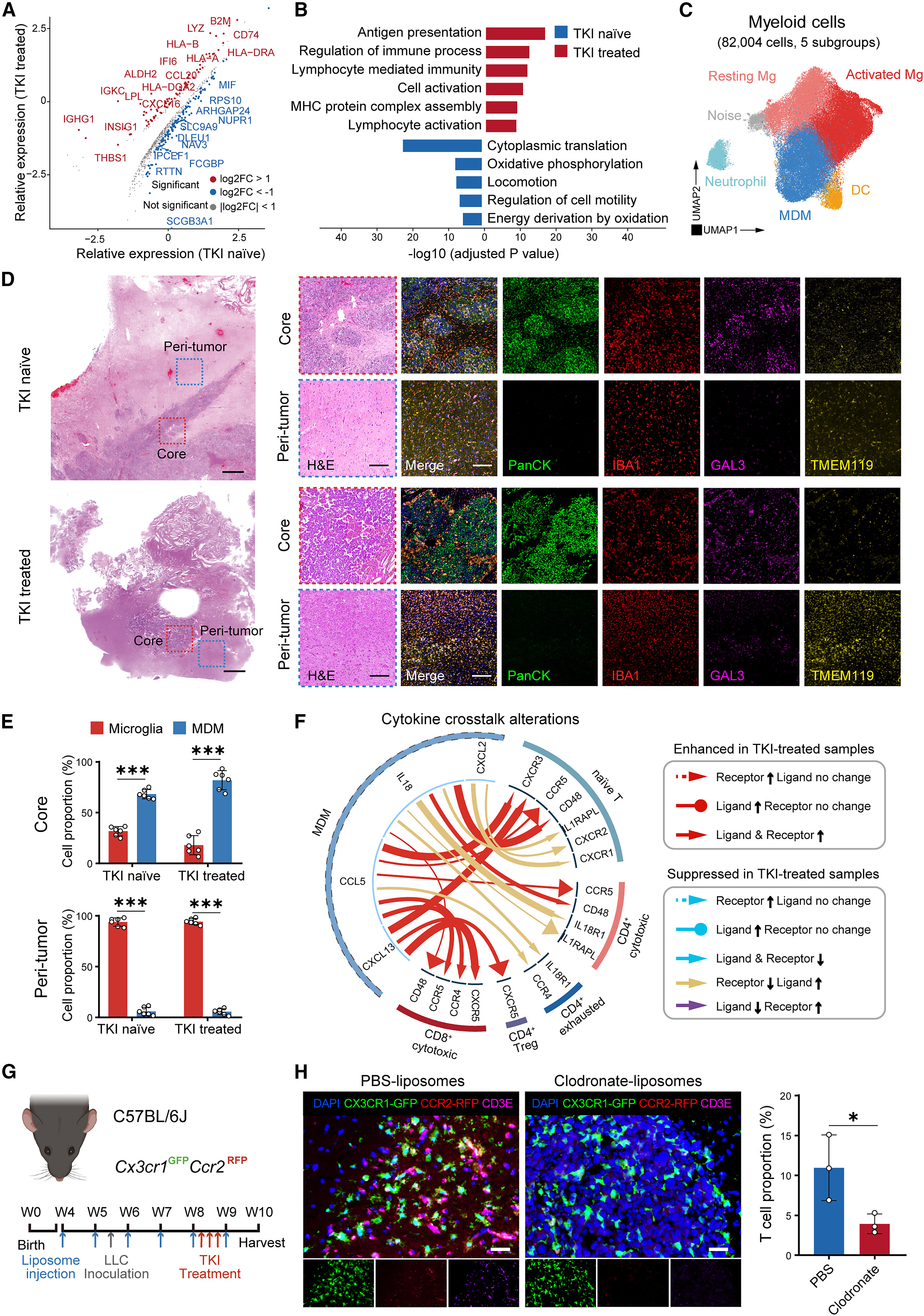
除了适应性免疫细胞,肿瘤相关髓系细胞(TAMs)在治疗诱导的免疫微环境重编程中也发挥关键作用。研究通过单细胞测序将髓系细胞分为5个亚群,其中单核细胞来源巨噬细胞(MDMs)和小胶质细胞是LCBM中最丰富的两个髓系亚群,分别占32.0%和56.9%。空间分布分析显示,MDMs在肿瘤核心区域更为富集,而小胶质细胞主要分布在肿瘤周围区域,提示MDMs可能直接引导T细胞进入肿瘤核心。
TKI治疗后,MDMs中人类白细胞抗原II类分子和趋化因子的表达显著升高,基因本体富集分析显示,抗原呈递和淋巴细胞介导的免疫相关通路被增强,说明MDMs可能参与TKI诱导的T细胞招募。细胞间相互作用分析显示,TKI治疗后,MDMs与T细胞之间的配体-受体相互作用显著增强。小鼠模型中,通过氯膦酸脂质体耗竭外周MDMs后,肿瘤核心区域的T细胞浸润显著减少。体外共培养实验进一步证实,TKI处理后的肿瘤细胞条件培养基可促进T细胞迁移,且MDMs分泌的趋化因子在其中发挥关键作用。这些结果表明,MDMs是TKI诱导T细胞浸润的核心介导者,为T细胞进入肿瘤微环境提供了必要的“桥梁”。
3、TKI诱导肿瘤细胞免疫原性死亡,并通过HMGB1/TLR/NF-κB轴调控免疫微环境
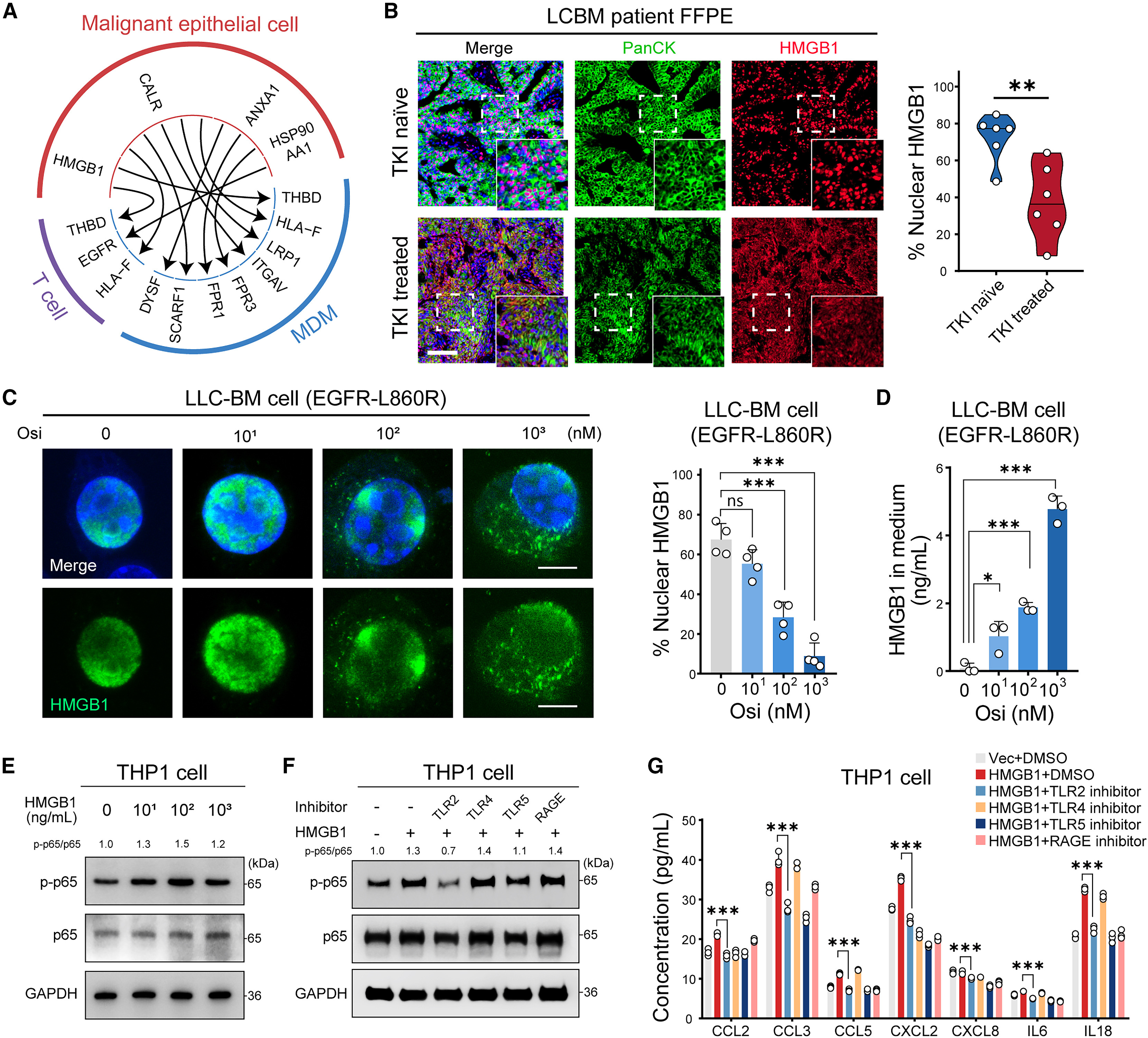
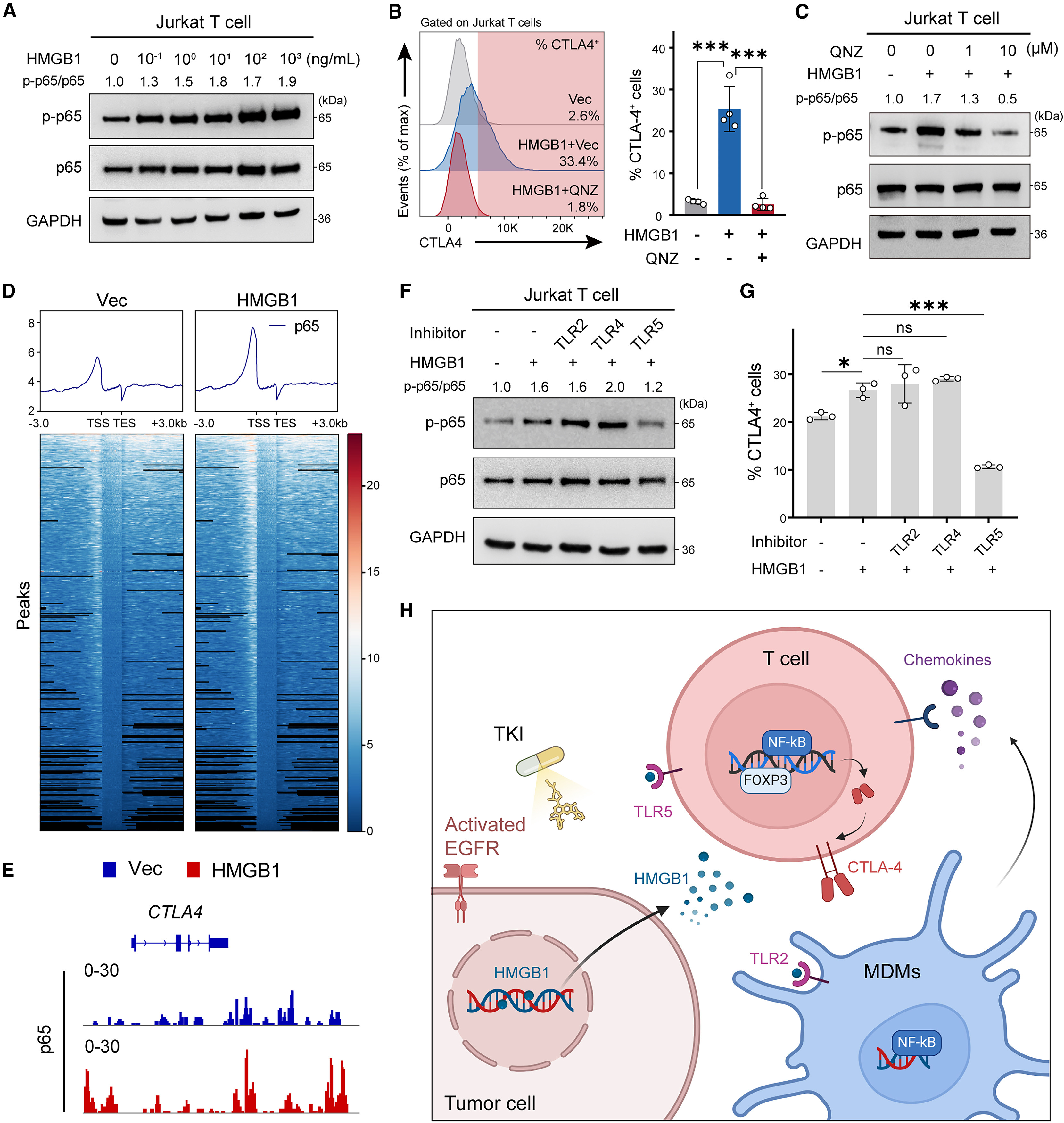
TKI已被证实可诱导肺癌细胞发生免疫原性死亡(ICD),而ICD释放的损伤相关分子模式(DAMPs)是连接肿瘤细胞与免疫细胞的关键信号。研究发现,TKI治疗后,肿瘤细胞会释放高迁移率族蛋白1(HMGB1)和钙网蛋白(CALR)等DAMPs,其中HMGB1的核定位比例显著减少,更多地释放到细胞外,且呈TKI剂量依赖性。体外实验显示,HMGB1可激活THP1来源巨噬细胞的NF-κB信号通路,而TLR2抑制剂(TLR2-IN-C29)可显著阻断这一激活过程,同时减少巨噬细胞趋化因子的释放,提示巨噬细胞通过TLR2识别HMGB1,启动下游信号通路并招募T细胞。
更重要的是,HMGB1也可作用于T细胞,以剂量依赖的方式激活T细胞的NF-κB信号通路,进而上调CTLA4的表达,而NF-κB抑制剂QNZ可逆转这一效应。CUT&Tag测序显示,HMGB1可促进NF-κB亚基p65结合到CTLA4的启动子区域,直接调控CTLA4的转录。进一步研究发现,T细胞通过TLR5识别HMGB1信号,TLR5抑制剂可显著降低CTLA4+ T细胞的比例。至此,研究勾勒出一条完整的调控通路:TKI诱导肿瘤细胞释放HMGB1,MDMs通过TLR2识别HMGB1并释放趋化因子招募T细胞,T细胞通过TLR5识别HMGB1后激活NF-κB信号,上调CTLA4表达,最终形成免疫抑制微环境,介导TKI耐药。
4、 CTLA4阻断与TKI协同作用,逆转免疫抑制并改善LCBM预后
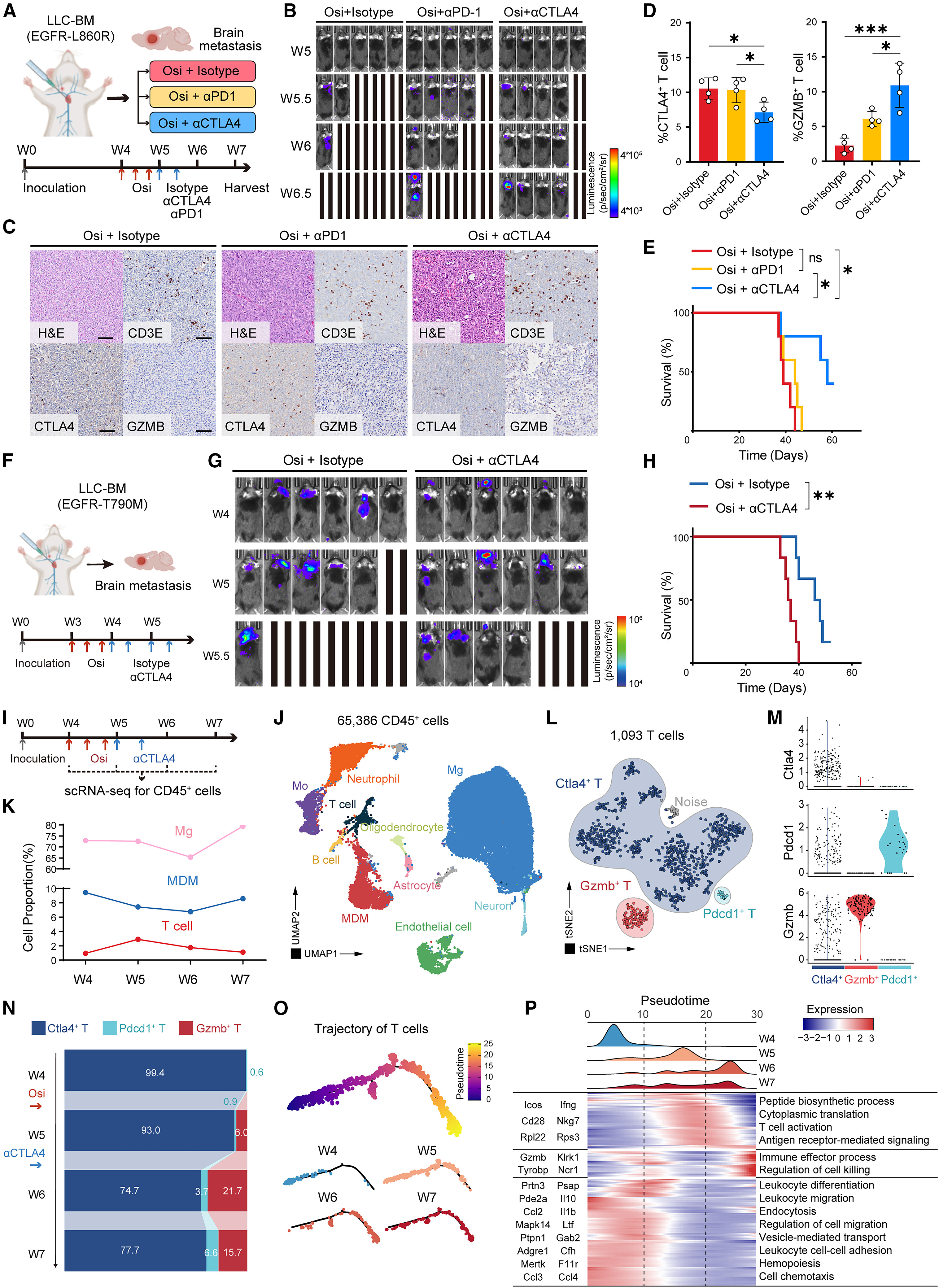
基于CTLA4在TKI诱导的免疫抑制中的核心作用,研究进一步验证了TKI联合CTLA4阻断的治疗效果。在模拟人类EGFR-L858R突变的LCBM小鼠模型中,TKI联合CTLA4阻断剂的序贯治疗,相比TKI单药治疗或TKI联合PD1阻断剂,可显著降低肿瘤负荷,减少CTLA4+ T细胞比例,同时增加GZMB+效应T细胞比例,并显著延长小鼠的总生存期。
在EGFR-T790M突变的LCBM小鼠模型中,TKI联合CTLA4阻断剂治疗同样显著改善小鼠生存期,且安全性良好,未出现严重的肝毒性或肺炎,血液生化指标基本维持在正常范围。时序单细胞测序分析显示,联合治疗过程中,免疫微环境经历了从T细胞功能障碍到T细胞复苏的动态转变:TKI治疗初期激活MDMs招募T细胞,但同时诱导CTLA4上调导致T细胞功能受损,加入CTLA4阻断剂后,CTLA4+ T细胞比例下降,GZMB+效应T细胞比例升高,T细胞的免疫效应功能显著增强,相关基因表达富集于免疫效应过程和细胞杀伤调控通路。
四、研究结论
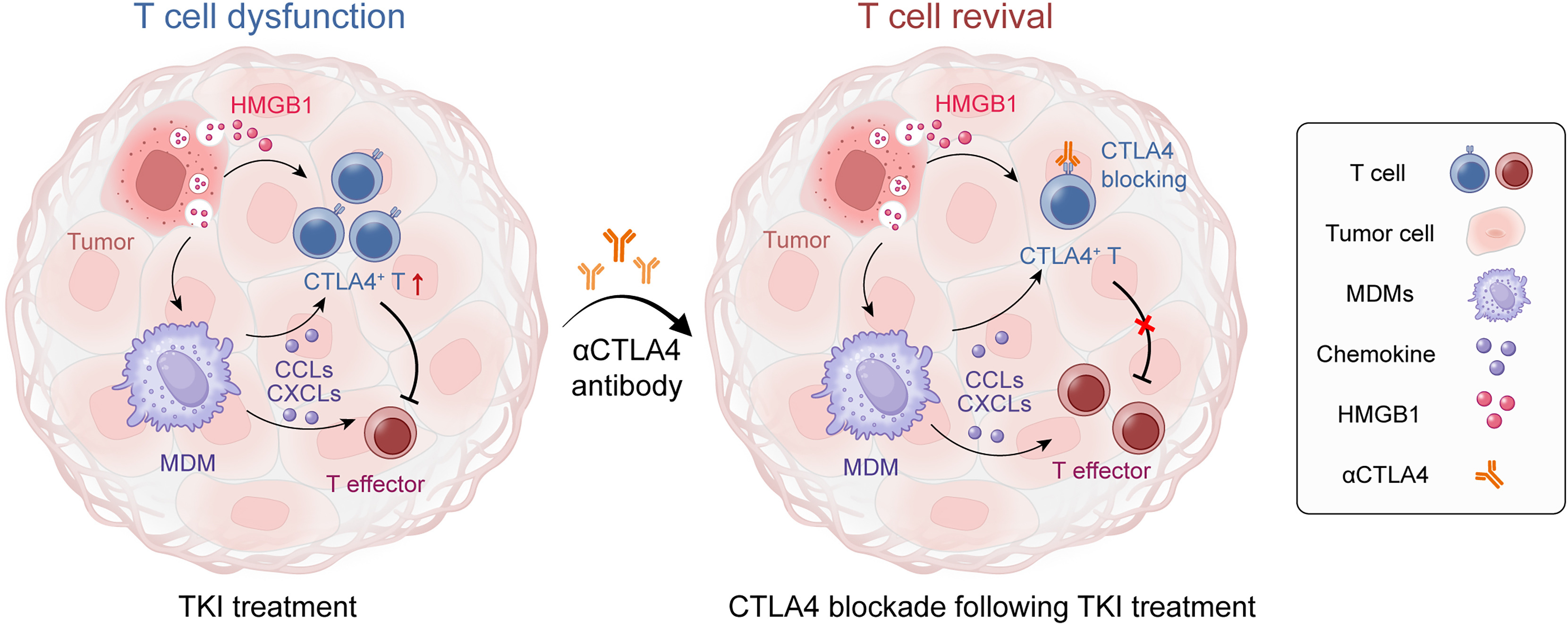
本研究首次系统揭示了TKI对EGFR突变型LCBM免疫微环境的双向调控作用:TKI通过激活MDMs招募T细胞,纠正T细胞缺乏的问题,但同时通过HMGB1/TLR/NF-κB轴上调CTLA4表达,诱导T细胞功能障碍,最终导致耐药。而CTLA4阻断可有效逆转这种免疫抑制,与TKI协同发挥抗肿瘤作用,无论在TKI敏感还是耐药突变的LCBM中均具有良好的治疗效果。该研究打破了对TKI耐药机制的传统认知,强调了免疫微环境重编程在耐药中的关键作用,为EGFR突变型LCBM的治疗提供了新的协同策略,也呼应了论文标题所聚焦的用CTLA4阻断克服肺癌脑转移中的TKI耐药这一核心主题。未来,需通过高质量临床研究进一步验证该联合方案的临床疗效,同时优化治疗时序和剂量,为晚期LCBM患者带来新的治疗希望。
参考文献
Fu M, Zhao J, Zhang L, Sheng Z, Li X, Qiu F, Feng Y, You M, Xu H, Zhang J, Zeng R, Huang Y, Li C, Chen W, Chen Z, Peng H, Li L, Wu Y, Ye D, Chi Y, Hua W, Mao Y. Overcoming tyrosine kinase inhibitor resistance in lung cancer brain metastasis with CTLA4 blockade. Cancer Cell. 2024 Nov 11;42(11):1882-1897.e7. doi: 10.1016/j.ccell.2024.09.012. Epub 2024 Oct 17. PMID: 39423817.
EnkiLife恩玑生命产品:
抗体标记试剂盒
Western Blot全流程实验方案
TSA多重荧光试剂盒
细胞荧光染料
稳转细胞系构建服务




