文献分享:整合应激反应经由LCN2介导肿瘤免疫逃逸
发表时间:2026-04-10一、研究背景
肿瘤免疫逃逸是制约癌症免疫治疗疗效的核心瓶颈,也是当前肿瘤免疫学领域的研究热点与难点。近年来,免疫检查点抑制剂(ICIs)等免疫治疗手段的问世,为多种实体瘤患者带来了新的治疗希望,但临床数据显示,仍有超过50%的患者对免疫治疗不响应或出现耐药,其根本原因在于肿瘤细胞通过多种分子机制逃避机体免疫系统的识别与清除。整合应激反应(Integrated Stress Response, ISR)作为细胞应对内质网应激、代谢压力等微环境胁迫的核心调控通路,在肿瘤细胞的存活、增殖及免疫逃逸过程中发挥着关键作用。其中,激活转录因子4(Activating Transcription Factor 4, ATF4)作为ISR下游最关键的转录因子,可通过调控下游靶基因的表达,参与肿瘤细胞的代谢重编程、抗凋亡及免疫抑制等多种生物学过程。已有研究证实,ATF4在肺癌、胰腺癌、黑色素瘤等多种恶性实体瘤中高表达,且其表达水平与肿瘤恶性程度、患者预后及免疫治疗耐药密切相关,但ATF4调控肿瘤免疫逃逸的具体分子机制、关键下游效应分子及其作用靶点,尚未被完全阐明,这也成为该领域基础研究向临床转化的重要瓶颈。由Bossowski J、Papagiannakopoulos T及Koide S等学者发表于国际顶级期刊《Nature》的研究《The integrated stress response promotes immune evasion through lipocalin 2》,针对这一亟待解决的科学问题展开了系统且深入的探究。该研究以肺癌、胰腺癌、黑色素瘤等临床常见且免疫治疗耐药率较高的实体瘤为研究对象,结合体内外实验、临床样本分析及大数据挖掘,首次揭示了脂钙蛋白2(Lipocalin 2, LCN2)作为整合应激反应下游的关键效应分子,介导肿瘤免疫逃逸的分子机制,并进一步证实靶向LCN2具有显著的抗肿瘤治疗潜力,为免疫治疗耐药的实体瘤提供了新的治疗方向与理论依据,该研究将基础研究与临床应用紧密结合,不仅填补了整合应激反应调控肿瘤免疫逃逸分子机制的研究空白,也为后续开发新型免疫治疗策略、改善肿瘤患者预后提供了重要的实验支撑与理论指导。
二、研究方法
为系统阐明整合应激反应通过LCN2介导肿瘤免疫逃逸的分子机制,明确LCN2的临床意义及靶向治疗潜力,本研究综合运用多种研究手段构建了多层次研究体系。研究以KP小鼠肺癌细胞、B16F10黑色素瘤细胞、KPC7胰腺癌细胞为核心对象,利用CRISPR-Cas9技术构建LCN2、ATF4敲除及过表达细胞系,结合定制的ATF4靶基因CRISPR-Cas9文库体内筛选、ChIP-qPCR、Western blot及ELISA等技术,验证整合应激反应-ATF4-LCN2调控轴及LCN2的分泌特性。动物实验方面,选用免疫正常的C57BL/6J小鼠与免疫缺陷的NSG小鼠构建移植瘤模型,结合KPC基因工程小鼠及诱导型shRNA沉默系统,探究LCN2在不同免疫环境及肿瘤不同阶段的作用。肿瘤微环境分析采用ExCITE-seq单细胞测序、流式细胞术、免疫荧光、IHC及LUMICKS AFS技术,解析LCN2对免疫细胞亚群的调控及与巨噬细胞受体SLC22A17的结合情况。临床验证结合TCGA泛癌数据库、肺腺癌及胰腺癌组织芯片,分析LCN2表达与临床特征、预后及免疫治疗响应的关联,同时开发LCN2特异性单克隆抗体,在多种肿瘤模型中验证其治疗效果与安全性。
三、结果分析
1. ATF4通过抑制抗肿瘤免疫驱动肿瘤进展
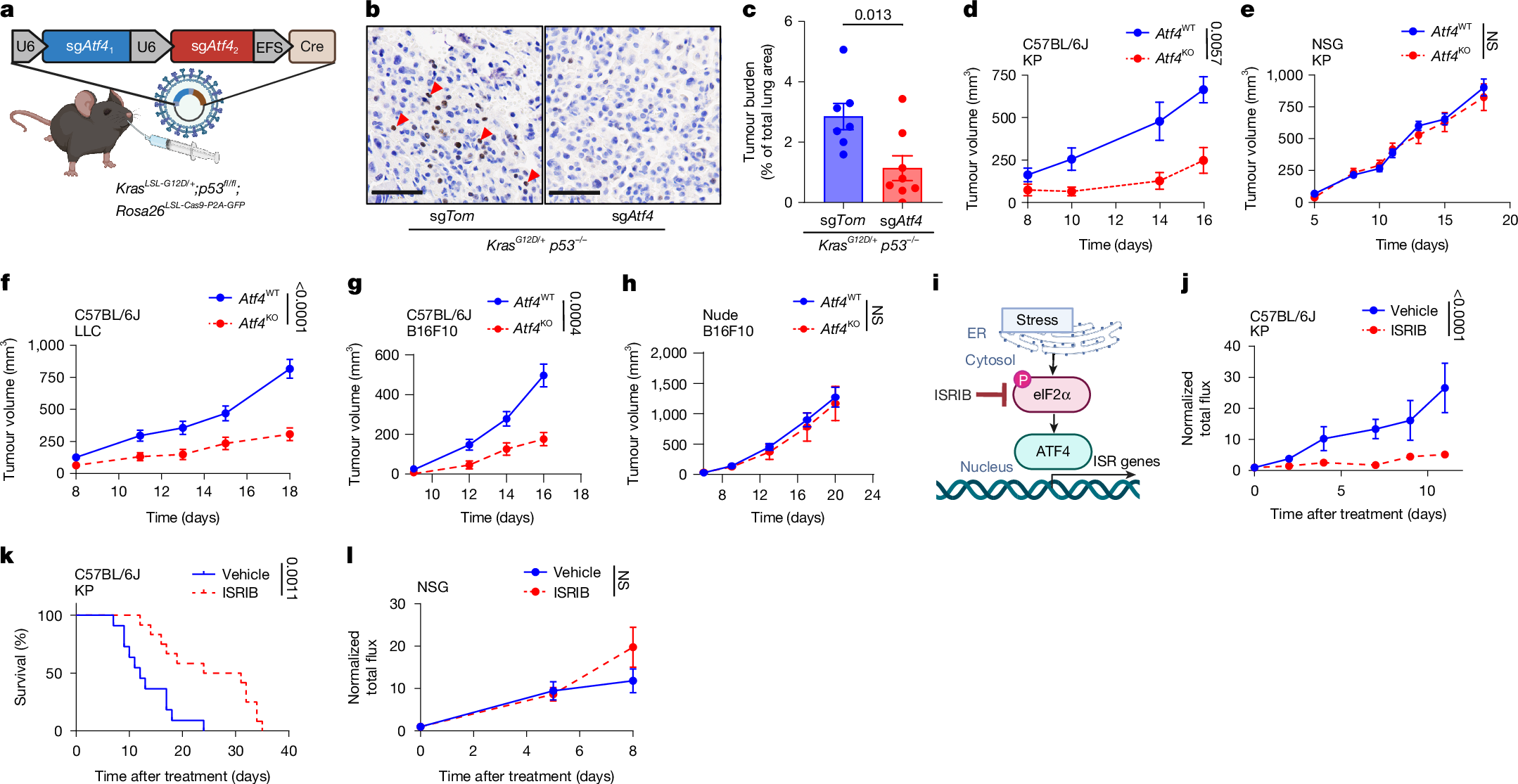
研究首先验证了ATF4在肿瘤进展中的核心作用,ATF4敲除的KP肺癌细胞在体外增殖能力与野生型细胞无显著差异,但在免疫功能正常的C57BL/6J小鼠体内,其肿瘤生长速度显著减慢,小鼠生存期明显延长。而在免疫缺陷的NSG小鼠体内,ATF4敲除与否对肿瘤生长无明显影响,这一现象提示ATF4的促肿瘤作用依赖于免疫系统。为进一步验证这一结论,研究使用ISR抑制剂ISRIB(可特异性拮抗磷酸化eIF2α,从而抑制ATF4活性)处理荷瘤小鼠,结果显示,ISRIB处理能显著抑制免疫功能正常小鼠的肿瘤生长、延长其生存期,却无法在NSG小鼠中发挥作用。这些结果串联起来,清晰地勾勒出ATF4的作用逻辑——它并非直接促进肿瘤细胞增殖,而是通过削弱机体的抗肿瘤免疫反应,为肿瘤生长保驾护航,也为后续探究ATF4调控免疫逃逸的下游分子靶点奠定了基础。
2. LCN2是ATF4介导免疫逃逸的关键下游靶点
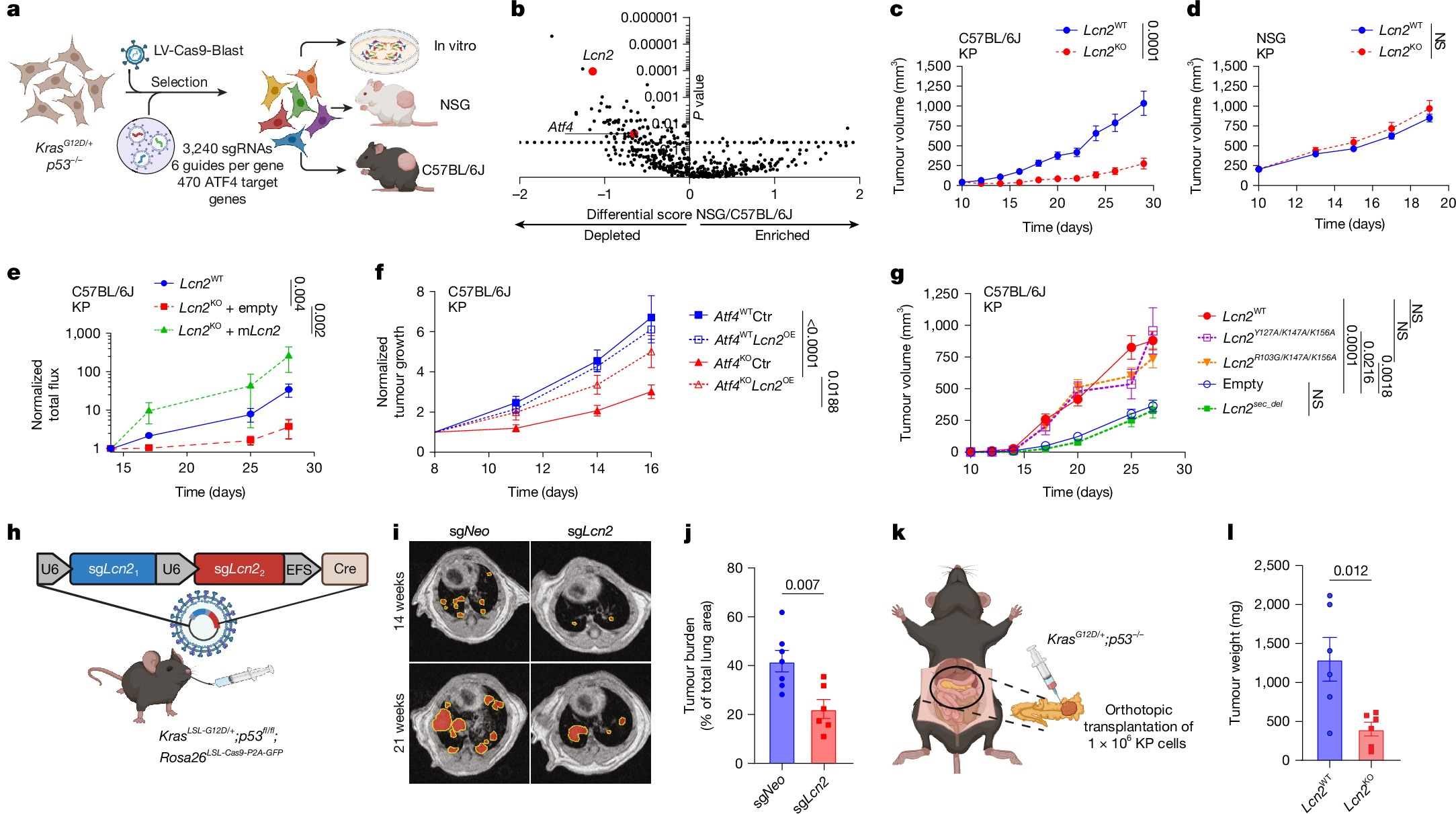
为找到ATF4驱动免疫抑制的关键因子,研究利用定制的CRISPR-Cas9文库(包含477个潜在ATF4靶基因),在C57BL/6J小鼠体内进行负向筛选,发现LCN2是除ATF4本身外,被显著消耗的基因之一,提示LCN2可能参与ATF4介导的免疫逃逸。后续实验进一步验证了这一猜想,与ATF4敲除的表型高度一致,LCN2敲除的KP细胞在C57BL/6J小鼠体内肿瘤生长显著受抑,而在NSG小鼠体内无明显差异。将LCN2重新导入LCN2敲除细胞,可恢复肿瘤生长能力,在ATF4敲除细胞中过表达LCN2,也能挽救其肿瘤生长缺陷,这直接证明LCN2是ATF4下游的关键效应分子,ATF4的免疫抑制作用依赖于LCN2。
进一步探究LCN2发挥作用的关键特征,研究构建了多种LCN2突变体:缺失分泌信号肽的突变体无法挽救LCN2敲除细胞的肿瘤生长缺陷,而丧失铁结合能力的LCN2突变体却能正常发挥作用,这表明LCN2的分泌功能是其免疫抑制作用的关键,而与铁结合能力无关。此外,在KPC基因工程小鼠模型中,通过CRISPR-Cas9敲除LCN2,可显著抑制肿瘤发生。在黑色素瘤、胰腺癌等其他实体瘤模型中,LCN2敲除也能抑制肿瘤生长,说明LCN2的免疫抑制作用具有跨肿瘤类型的普遍性。更重要的是,利用强力霉素诱导的shRNA沉默已建立肿瘤中的LCN2,可显著减慢肿瘤生长、延长小鼠生存期,提示LCN2是晚期肿瘤的潜在治疗靶点。
3. ISR-ATF4轴直接调控LCN2表达
研究进一步明确了ATF4调控LCN2表达的分子机制,经典的ISR诱导剂可显著上调ATF4蛋白水平及LCN2表达,而这种诱导作用在ATF4敲除细胞中完全消失。ISRIB处理可阻断ISR诱导剂对LCN2的上调作用,但不影响NF-κB通路介导的LCN2表达,说明LCN2的表达受ISR-ATF4轴特异性调控。临床相关代谢抑制剂,如谷氨酰胺酶抑制剂CB-839、线粒体呼吸抑制剂苯乙双胍也能诱导LCN2表达,且这种诱导依赖于ATF4。体内实验中,苯乙双胍处理可增加荷瘤小鼠肿瘤细胞中LCN2的表达,且与ATF4阳性细胞比例正相关,而ISRIB处理则会降低ATF4阳性细胞比例。
ChIP-qPCR实验证实,ATF4可直接结合到LCN2的启动子区域,与已知的ATF4靶基因Chac1、Asns类似,进一步验证了ATF4对LCN2的直接转录调控作用。TCGA数据库分析显示,在肺癌、胰腺癌、黑色素瘤中,LCN2表达与ATF4转录特征高度相关。在非小细胞肺癌中,LCN2表达还与NF-κB特征正相关,提示LCN2的表达受ATF4和NF-κB两条通路共同调控,但ATF4介导的调控在肿瘤免疫逃逸中发挥主导作用。
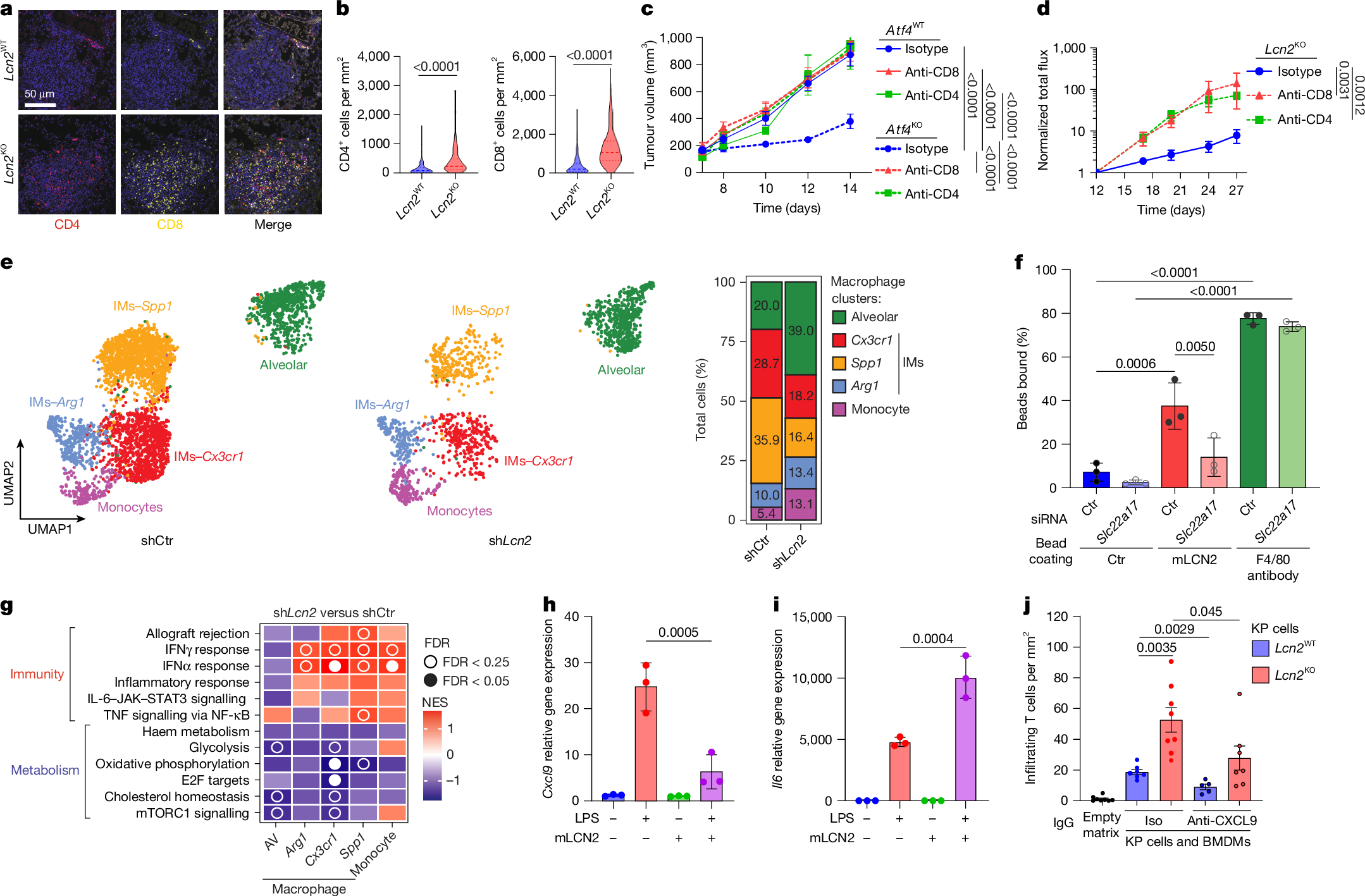
4. LCN2通过调控巨噬细胞表型抑制T细胞介导的抗肿瘤免疫
既然LCN2是分泌型蛋白,其免疫抑制作用必然通过调控肿瘤微环境中的免疫细胞实现。研究发现,LCN2敲除的肺癌肿瘤中,CD4+、CD8+肿瘤浸润淋巴细胞(TILs)数量显著增加,而具有免疫抑制功能的CD4+FOXP3+调节性T细胞(Treg)数量显著减少。ISRIB处理也能模拟这一表型,增加CD8+TILs浸润。更重要的是,耗尽CD4+或CD8+T细胞后,ATF4敲除和LCN2敲除带来的肿瘤生长抑制效应完全消失,说明T细胞是LCN2介导免疫逃逸的核心靶点。
ExCITE-seq单细胞分析进一步揭示了LCN2对肿瘤微环境中免疫细胞的调控细节,LCN2沉默后,肿瘤中巨噬细胞和中性粒细胞比例降低,肺泡巨噬细胞(AMs)比例升高,而间质巨噬细胞(IMs)亚群比例降低。进一步研究发现,LCN2的受体SLC22A17主要在巨噬细胞中表达,LUMICKS AFS实验证实,LCN2可通过结合SLC22A17与巨噬细胞相互作用。功能分析显示,LCN2可抑制巨噬细胞中抗瘤因子CXCL9的表达,促进促瘤因子IL-6的表达,从而抑制T细胞浸润,而敲除SLC22A17可阻断LCN2对巨噬细胞的调控作用。3D共培养实验进一步验证,LCN2敲除细胞可促进CD8+T细胞浸润,而中和CXCL9可显著削弱这一效应,完整揭示了LCN2的作用链条:肿瘤细胞分泌的LCN2结合巨噬细胞表面的SLC22A17,调控巨噬细胞表型,抑制CXCL9分泌,从而减少T细胞浸润,实现免疫逃逸。
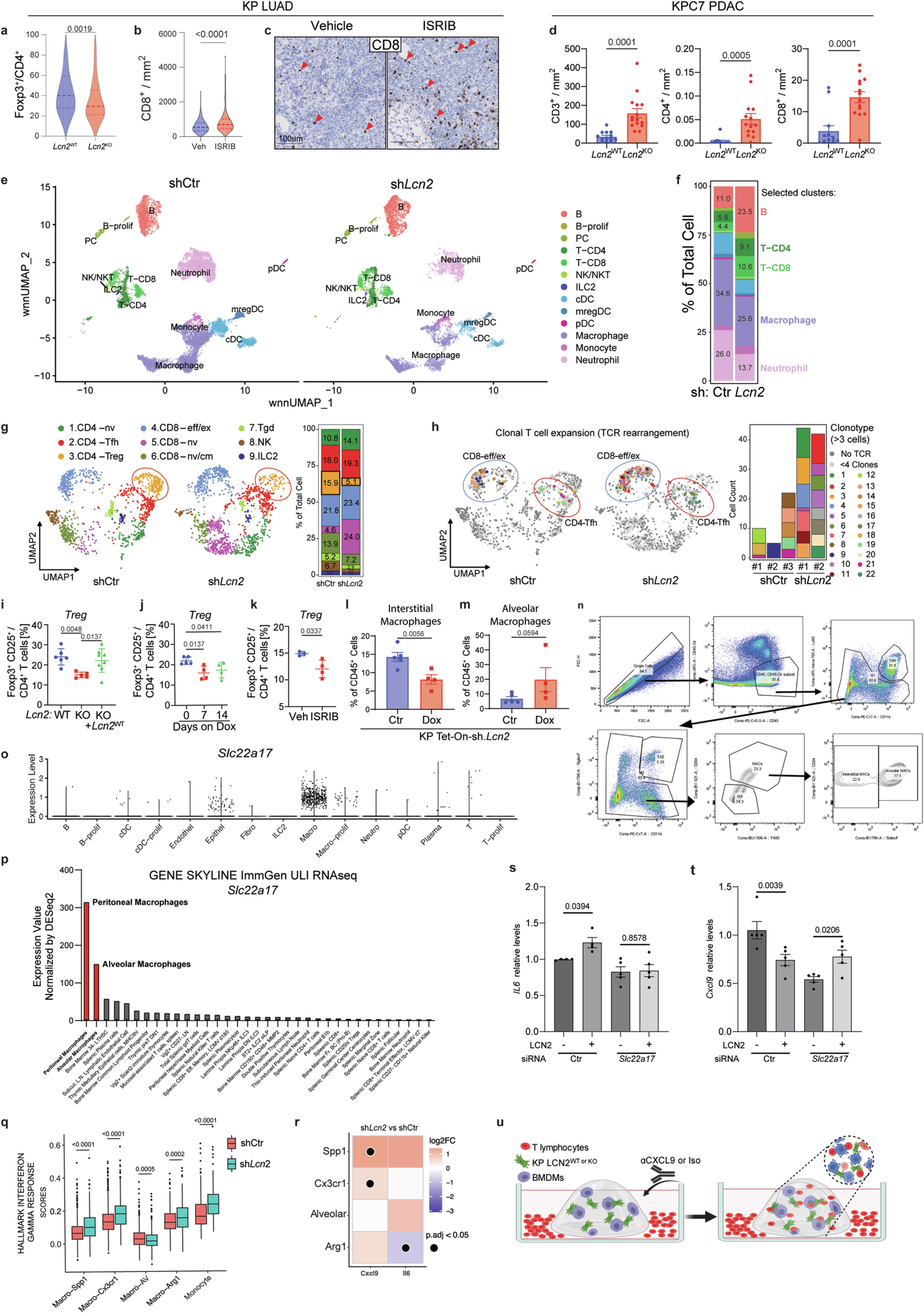
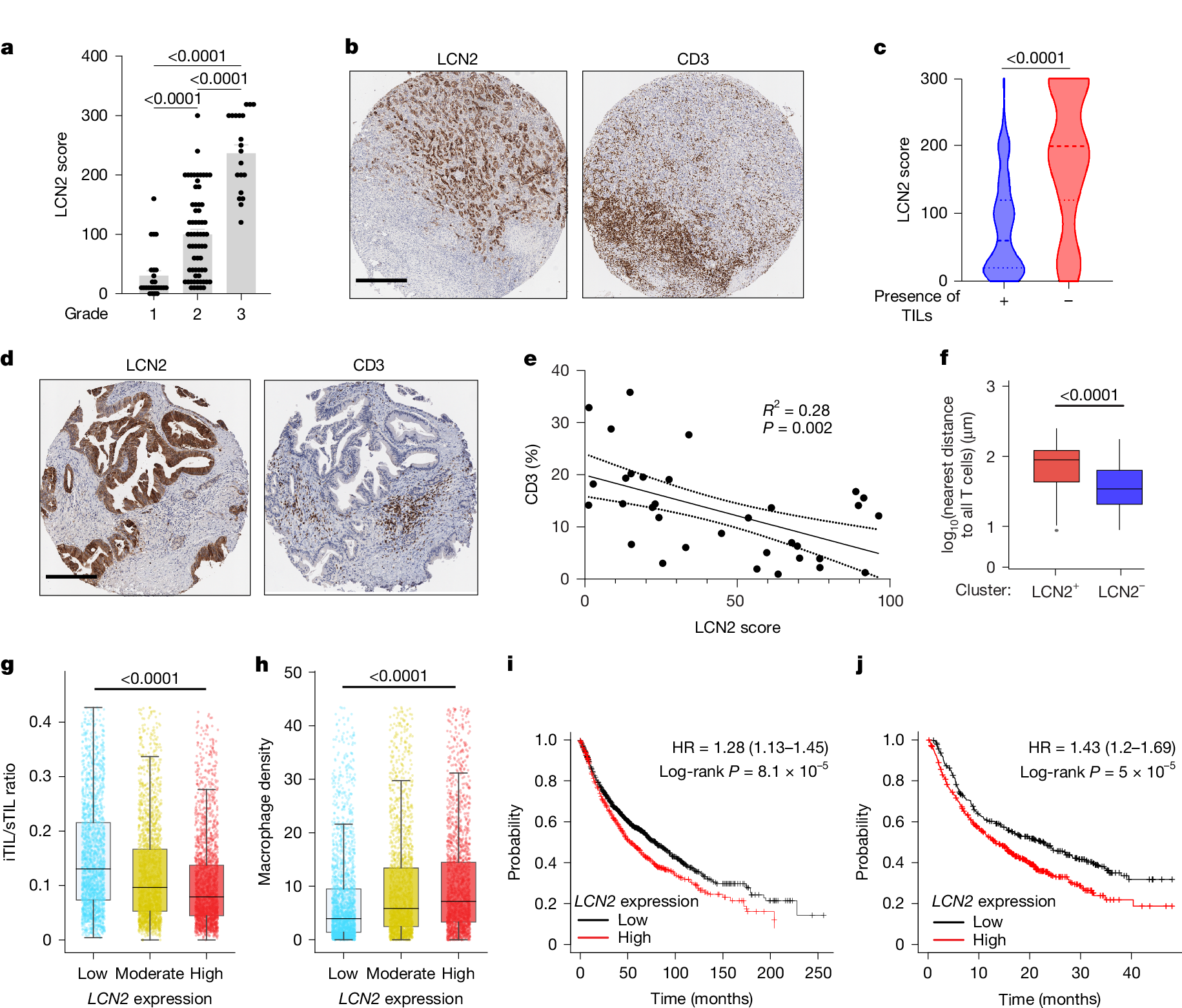
5. LCN2与人类肿瘤恶性程度及免疫治疗响应密切相关
为明确LCN2的临床意义,研究对105例肺腺癌患者的肿瘤组织芯片进行分析,发现LCN2表达水平与肿瘤分级显著正相关,肿瘤分级越高,LCN2表达越强。且LCN2高表达区域往往伴随CD3+T细胞浸润减少,LCN2高表达患者的TILs阳性率显著低于低表达患者。在33例胰腺癌患者样本中,也观察到LCN2表达与CD3+T细胞浸润呈负相关的现象。单细胞空间分析显示,LCN2阳性细胞周围T细胞的空间排斥性显著增加,提示LCN2在肿瘤局部发挥免疫抑制作用。
TCGA泛癌分析显示,LCN2和ATF4在免疫排斥型肿瘤中的表达显著高于炎症型肿瘤,LCN2高表达组的肿瘤内T细胞与基质T细胞比例(iTIL/sTIL)显著降低,而巨噬细胞密度显著升高,与小鼠模型结果一致。生存分析显示,LCN2高表达的肺癌患者中位生存期显著短于低表达患者,胰腺癌患者中也存在类似趋势。在接受免疫治疗的癌症患者中,LCN2低表达组的生存期显著长于高表达组,提示LCN2可作为预测免疫治疗响应的潜在生物标志物。
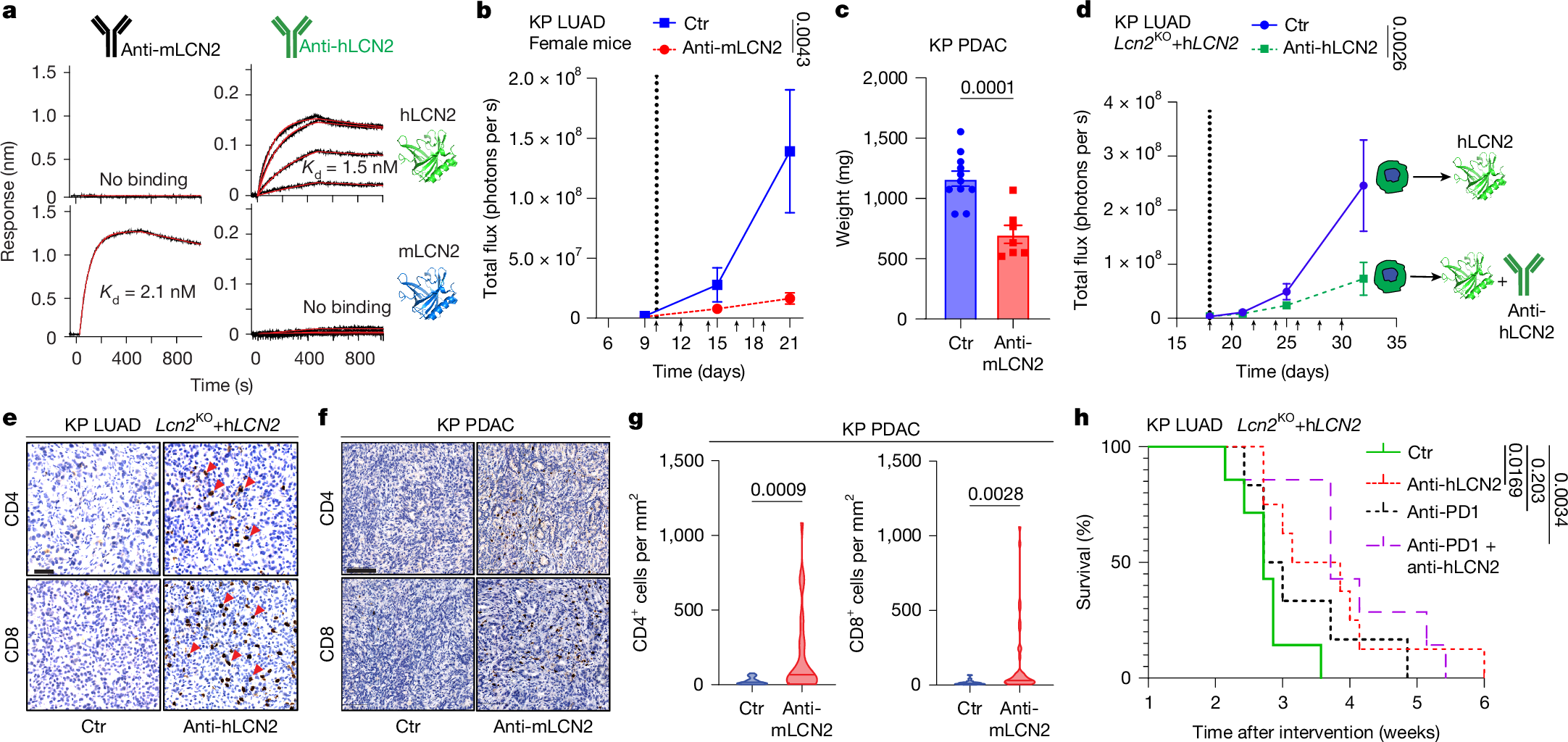
6. LCN2特异性抗体具有显著的抗肿瘤治疗效果
基于LCN2的分泌特性和临床意义,研究开发了针对小鼠LCN2(mLCN2)和人类LCN2(hLCN2)的特异性抗体。在免疫原性肿瘤模型(雄性原发肿瘤细胞移植到雌性小鼠)中,抗mLCN2抗体处理可显著抑制原位肿瘤生长,延长小鼠生存期。在对免疫检查点抑制剂耐药的冷肿瘤模型(雄性小鼠移植KP肺癌细胞)中,抗mLCN2抗体也能有效抑制肿瘤生长,且不影响小鼠外周血中淋巴细胞、中性粒细胞等免疫细胞数量,无明显急性毒性。在胰腺癌原位移植模型中,抗mLCN2抗体同样表现出显著的抗肿瘤效果。
为验证抗hLCN2抗体的治疗潜力,研究构建了表达hLCN2的LCN2敲除KP细胞模型,发现抗hLCN2抗体可显著抑制该模型的肿瘤生长,增加肿瘤中CD4+、CD8+T细胞浸润,减少Treg细胞数量。同时,抗hLCN2抗体可恢复巨噬细胞中CXCL9的表达,抑制IL-6的表达,逆转LCN2介导的免疫抑制微环境。这些结果表明,LCN2特异性抗体可通过阻断LCN2的免疫抑制作用,激活机体抗肿瘤免疫,为临床治疗免疫排斥型实体瘤提供了新的策略。
四、研究总结
本研究通过系统的体内外实验,首次揭示了ISR-ATF4-LCN2轴介导肿瘤免疫逃逸的分子机制,即ATF4作为ISR下游关键转录因子,直接结合LCN2启动子并调控其分泌,肿瘤细胞分泌的LCN2通过结合巨噬细胞表面的SLC22A17,调控巨噬细胞表型,抑制CXCL9分泌,减少T细胞浸润,从而促进肿瘤免疫逃逸。研究同时证实,LCN2表达与人类实体瘤的恶性程度、T细胞浸润及免疫治疗响应密切相关,靶向LCN2的特异性抗体具有显著的抗肿瘤效果且安全性良好。该研究不仅填补了ATF4调控肿瘤免疫逃逸的分子机制空白,还为免疫治疗耐药的肺癌、胰腺癌等实体瘤提供了新的治疗靶点和生物标志物,具有重要的基础研究价值和临床转化前景。
参考文献
Bossowski JP, Pillai R, Kilian J, Wong Lau A, Nakamura M, Rashidfarrokhi A, Hao Y, Li R, Wu K, Hattori T, Glasser E, Koide A, Wang L, Moreira AL, Hajdu C, Rajalingam S, LeBoeuf SE, Le H, Lee S, Oh JW, Joe C, Kim H, Ock CY, Lee SH, Wang H, Patel AAH, Sayin VI, Tsirigos A, Wong KK, Koralov SB, Pende M, Sánchez-Rivera FJ, Simeone DM, Zervantonakis IK, Koide S, Papagiannakopoulos T. The integrated stress response promotes immune evasion through lipocalin 2. Nature. 2026 Feb 18. doi: 10.1038/s41586-026-10143-0. Epub ahead of print. PMID: 41708864.
2h极速WB即用型全流程试剂盒: